随着科学技术的不断进步和创新,原发性肿瘤模型的研究和应用也将迎来新的发展机遇。以下是一些发展趋势:精细化与个体化:未来的原发性肿瘤模型将更加注重精细化与个体化,例如通过单细胞测序等技术分析tumour细胞的异质性,以及根据患者的基因组信息建立个体化肿瘤模型等。多学科交叉融合:tumour学研究涉及到多个学科领域,包括细胞生物学、分子生物学、免疫学、药理学等。未来的原发性肿瘤模型将更加注重多学科交叉融合,以推动研究工作的深入发展。通过肿瘤模型可以评估不同调理方案在抑制tumour生长方面的效果。南京干细胞肿瘤模型实验研究

肿瘤模型在生物医学研究中的重要作用:通过模拟患者的tumour基因表达情况,研究人员可以预测患者对不同药物的反应,从而选择可能有效的药物进行调理。此外,肿瘤模型还可以用于测试特定基因变异对tumour生长和发展的影响,进一步深化我们对tumour生物学的理解,为开发新的调理策略提供线索。跨物种模型的应用:除了传统的动物模型外,研究人员还在努力开发跨物种的肿瘤模型,如人源化的小鼠模型和人类细胞系模型等。这些模型能够更好地模拟人类的tumour生长和生物学特性,为抗tumour药物的研发提供更准确的预测。此外,跨物种模型还可以用于研究人类和动物之间的tumour转移差异,从而揭示潜在的进化差异和新的调理靶点。北京肿瘤模型检测肿瘤模型可以用于评估放射调理的疗效。
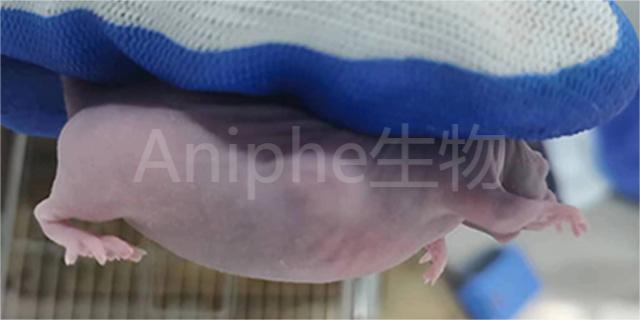
肿瘤模型在生物医学研究中的重要作用:免疫调理模型的评估。免疫调理是近年来tumour调理的研究热点之一。通过建立免疫调理模型,研究人员可以评估不同免疫调理方案的效果,如免疫检查点抑制剂、CAR-T细胞疗法等。此外,免疫调理模型还可以用于研究免疫细胞与tumour细胞之间的相互作用机制,从而揭示新的调理靶点和免疫逃逸机制。肿瘤模型在生物医学研究中具有非常重要的作用。通过模拟人类tumour的生长和生物学特性,肿瘤模型为我们提供了理解tumour发生和发展机制的重要工具。同时,利用肿瘤模型进行药物筛选和评估、预测耐药性和优化临床试验设计等方面也具有广泛的应用价值。随着技术的不断进步和新模型的研发,我们有理由相信未来肿瘤模型将在生物医学研究中发挥更大的作用,为人类战胜病症这一顽疾提供更多的帮助和支持。
尽管肿瘤模型的建立和研究取得了明显的进展,但仍面临着许多挑战。首先,每种模型都有其局限性,无法完全模拟真实的tumour生长和转移过程。例如,原位移植模型虽然能模拟tumour的自然生长环境,但动物个体差异以及复杂的宿主反应可能会影响实验结果的稳定性。细胞系模型虽然为大规模药物筛选提供了便利,但常常忽略了个体差异和tumour异质性。基因工程模型可以模拟基因突变对tumour发生的发展影响,但在复杂的tumour微环境中,基因突变并非是单独的致病因素。免疫模型可以模拟免疫系统对tumour的影响,但在免疫抑制或免疫启动的微环境中,免疫反应的复杂性仍然是一个挑战。肿瘤模型可以用于研究tumour的微环境和血液供应。
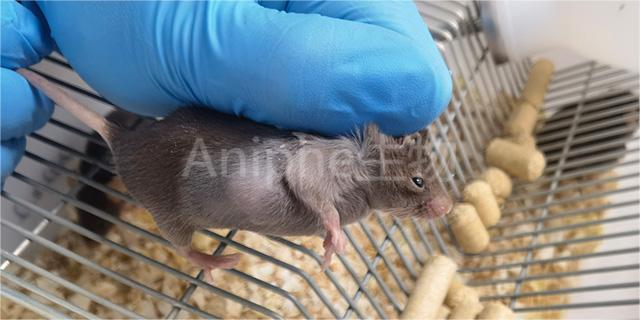
原发性肿瘤模型的发展趋势:临床转化与实际应用:未来的原发性肿瘤模型将更加注重与临床实践的结合,实现从实验室到临床的转化。例如,通过建立与临床实践相似的动物模型,可以模拟患者对不同调理策略的反应和预后情况,为个体化调理提供依据;同时,这些模型还可以用于测试新型抗tumour药物的疗效和安全性,为新药研发提供支持。原发性肿瘤模型作为研究tumour发生、发展机制的重要工具,具有广泛的应用价值和发展前景。未来的研究将更加注重精细化、个体化和多学科交叉融合,同时新型技术的应用和临床转化将成为研究的重要方向。相信随着技术的不断进步和创新,原发性肿瘤模型将在未来的tumour学研究中发挥更加重要的作用。通过肿瘤模型,科学家可以寻找新的药物靶点和调理策略。南京干细胞肿瘤模型实验研究
肿瘤模型可以用于测试tumour预防和调理方法的有效性。南京干细胞肿瘤模型实验研究
制备移植性肿瘤模型通常采用以下步骤:首先,选择适合的实验小鼠和人类或动物的源tumour细胞;其次,将源tumour细胞接种到实验小鼠的适宜部位,如皮下、肌肉或内脏部位等;然后,经过一定时间后,源tumour细胞会在实验小鼠体内生长和转移,形成移植性肿瘤模型。在制备过程中,需要对源tumour细胞的生物学特性、遗传背景、分化程度、免疫原性等进行详细的分析和评估,以确保模型的可靠性和稳定性。深入探讨tumour生物学特性:通过制备小鼠肿瘤模型,可以模拟人类tumour的发生和发展过程,从而深入探讨tumour的生物学特性、细胞增殖和凋亡机制、基因突变和表观遗传学改变等。这些研究有助于更好地理解tumour的发生和发展机制,为抗tumour药物的研发提供理论依据。南京干细胞肿瘤模型实验研究