- 品牌
- 世途科生物
- 型号
- CM0001
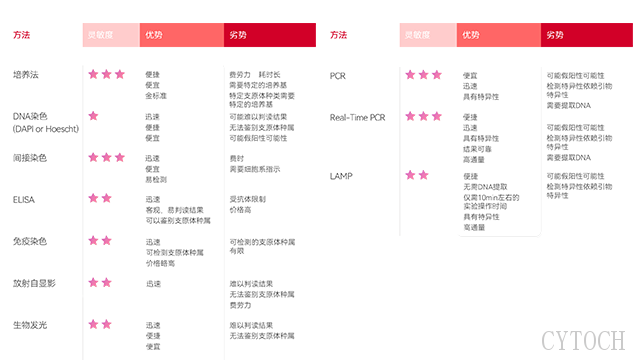
qPCR法,即定量聚合酶链式反应(QuantitativePolymeraseChainReaction)法,在支原体检测中的应用主要体现在以下几个方面:
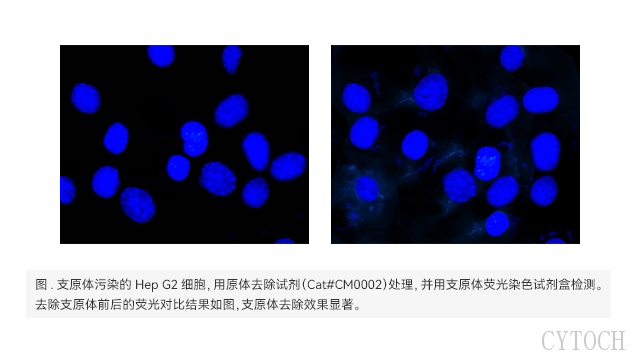

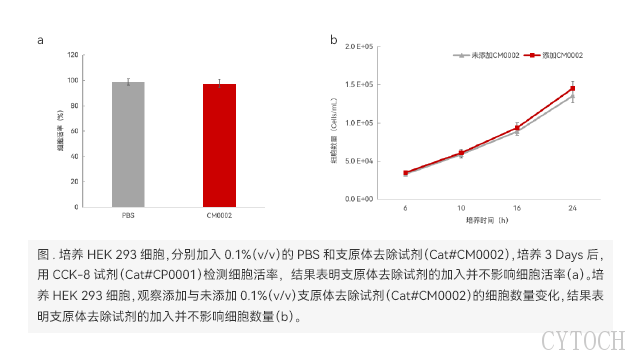
一步法快速支原体检测的原理?支原体去除货期
在CYTOCH的理念中,化学与生物的结合是提升产品性能的关键。化学技术的进步为生物医学领域提供了更多的可能性,使得相关实验结果更为灵敏、准确。为了在细胞研究领域取得技术性突破,CYTOCH研发团队不断尝试将新型的化学技术与生物技术相融合。CYTOCH在细胞领域所进行的已有技术的持续突破、新技术的创新研发、化学与生物技术的不断碰撞结合,使得CYTOCH产品在临床诊断、药物研发和科研教育等领域都具有广泛的应用前景。
在保证研发驱动力的前提下,为确保产品质量的稳定与可靠以及产品的使用性,CYTOCH对原料供应商进行严格审计和把关,选择品质优良的原料进行后续产品生产。 在生产过程中,CYTOCH对生产人员资质、生产环境、生产过程、生产物料进行严格把控。后续的产品质检、入库出库均严格按照企业内控标准由质量和仓库物流人员进行层层把关,确保每一批出厂产品质量都处于行业前端水平。
在方面,由于支原体没有细胞壁,因此一些针对细胞壁的对其无效。通常会选用大环内酯类、四环素类等进行。同时,患者在期间也需要注意休息、加强营养,提高自身的。总之,支原体虽然微小,但却不可忽视。我们应该加强对支原体的认识,提高对支原体的警惕性,做到早发现、早诊断、早,以保障我们的身体健康。在细胞培养的过程中,支原体污染是一个常见而又棘手的问题。为了确保细胞培养的质量和可靠性,进行细胞支原体检测至关重要。支原体体积微小,却能对细胞造成损害,干扰正常生理功能。南京细胞支原体检测方法等温扩增在微生物的广袤天地中,支原体宛如一群神秘的小精灵,隐匿在我们肉眼难以察觉的微观世界里。它们虽微小,却蕴含着巨大的生物...
- 上海细胞支原体去除试剂价格 2024-12-04
- 温州支原体去除现货 2024-12-04
- 北京细胞培养支原体预防试剂现货 2024-12-04
- 深圳支原体预防价格 2024-12-04
- 广州细胞培养支原体检测说明书 2024-12-04
- 上海支原体检测试剂货期 2024-12-04
- 上海细胞支原体去除 2024-12-04
- 上海细胞培养支原体去除试剂价格 2024-12-04
- 深圳支原体检测方法等温扩增 2024-12-03
- 杭州细胞支原体预防试剂多少钱 2024-12-03
- 广州支原体检测试剂现货 2024-12-03
- 上海支原体检测要多久 2024-12-03
- 细胞培养支原体检测说明书 2024-12-03
- 苏州细胞培养支原体检测方法 2024-12-03
- 南京细胞培养支原体检测方法 2024-12-02
- 北京细胞培养支原体预防现货 2024-12-02


- 北京细胞培养支原体预防试剂现货 12-04
- 深圳支原体预防价格 12-04
- 苏州Co IP免疫沉淀选磁珠还是琼脂糖珠 12-04
- 广州细胞培养支原体检测说明书 12-04
- 深圳IP免疫沉淀选磁珠还是琼脂糖珠 12-04
- 上海支原体检测试剂货期 12-04
- 上海细胞支原体去除 12-04
- 杭州IP免疫沉淀磁珠货期 12-04
- 上海细胞培养支原体去除试剂价格 12-04
- 苏州蛋白免疫沉淀磁珠应用 12-03