阴离子脂体由带负电荷的脂质组成,如磷脂酰甘油、磷脂酰丝氨酸和磷脂酸,由于它们被巨噬细胞摄取,循环时间缩短。带负电的小脂质体比其对应的中性和带正电的脂质体被***得更快。此外,在带负电荷的小脂质体中观察到一种双相***模式。 另一方面, 与中性和带正电的脂质体相比, 血液单核细胞和肺在带负电的大脂质体的摄取中起主要作用。表面修饰的脂质体(携带配体)比天然脂质体更容易被***。 然而, 脂质体通过掺入胆固醇可在一定程度上减少肝脏对脂质体的摄取, 这可能会使磷脂包装转变为更坚硬有序的膜。脂质体疫苗可以机器体内的免疫应答。内蒙古北京脂质体载药
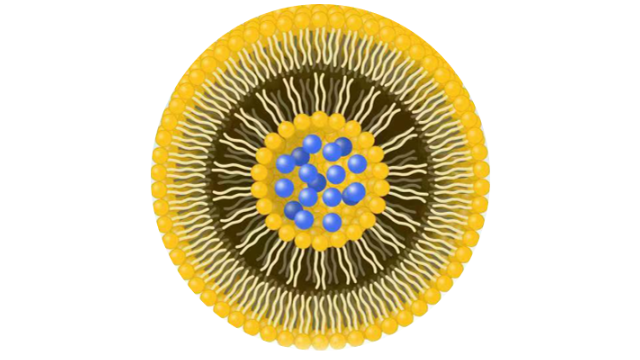
脂质体的粒径和粒径分布脂质体的整个药代动⼒学过程,如全⾝循环和MPS***、外渗到组织间质、细胞外基质间质运输以及细胞摄取和细胞内运输,都是依赖于尺⼨的。粒径<200nm的颗粒可降低⾎清蛋⽩的调理作⽤,降低MPS的***率。在⼩⿏⽩⾎病模型中,对于Myocet来说,较⼩的脂质体具有更⾼的抗**功效和增加的平均⽣存时间。粒径为2.0-3.5µm的Mepact可促使单核细胞/巨噬细胞吞噬,触发*****的免疫调节作⽤。Singh等⼈发现,含有不同颗粒⼤⼩的佐剂脂质体(ArmyLiposomeFormulation,ALF)的疫苗会产⽣不同的免疫反应,即树突状细胞更有效地摄取10-200nm范围内的⼩颗粒,⽽其他免疫细胞,如巨噬细胞,则倾向于吞噬⼤颗粒。Niu等⼈研究了⼝服给药的胰岛素负载脂质体,发现直径为150nm和400nm的脂质体表现出较慢且持续时间⻓达24⼩时的降糖作⽤,⽽粒径约为80nm和2µm的脂质体则分别表现出短暂且⽆药理作⽤。文献表明,对于*****的脂质体来说,小于200nm的脂质囊泡大小可以从物理肝脏筛选过程中逃逸。根据肝窦的大小,需要小于150nm的囊泡才能通过高渗透性的**血管穿透到恶性组织中。因此,它是由增强的渗透率(EPR)效应控制的,这有助于脂质体通过被动靶向在**中积累。内蒙古北京脂质体载药PEG2000是一种聚乙二醇(PEG)衍生物,常用于脂质体的表面修饰。
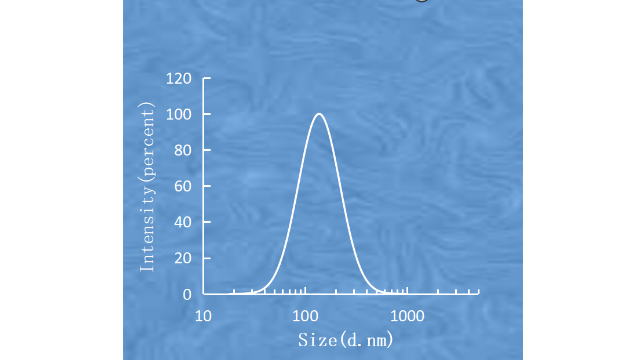
脂质体成分配比脂质体是由多种组分构成的,
主要包括:1.磷脂质:是脂质体**主要的组分,构成了脂质双层结构的主体。磷脂质包括磷脂、甘油磷脂、胆固醇等,它们在水性环境中通过亲水头部和疏水尾部的相互作用形成了双层结构。2.胆固醇:在脂质体中扮演着调节脂质双层流动性和稳定性的重要角色。胆固醇可以调节磷脂质的包装密度,增强脂质体的机械稳定性。3.表面活性剂:通常用于稳定脂质体的水合壳,并且有助于脂质体的稳定分散在水相中。常见的表面活性剂包括辛酸单酯类、磺酸盐类等。4.PEG衍生物:如前面所述,聚乙二醇(PEG)衍生物可以修饰脂质体表面,增强其稳定性、延长血液循环时间和降低免疫原性。5.药物或其他活性成分:脂质体通常被设计用来载药或其他活性成分,这些物质可以被包裹在脂质体内部,通过脂质双层的特性来实现针对性的释放或传递。DepoCyte、DepoDur和Exparel具有特殊的结构和相似的脂质成分。MVLs的形成⾄少需要两种类型的脂质:两亲性脂质和中性脂质(如双⽢油酯、⽢油三酯、植物油)。
酸性环境(pH值2.0-4.0)通常⽤于产⽣⽤于活***物装载的跨膜pH梯度。在37℃和pH2.0条件下,SM/Chol脂质体(55/45,mol/mol)的⽔解速率⽐DSPC/Chol脂质体慢约100倍。此外,含有SM/Chol的脂质体表现出比较好的药代动⼒学特性,即增加循环时间并增强药物向靶组织的递送。胆固醇(Chol)是脂质体双分⼦层的另⼀个主要成分,⼏乎可以⽤于所有的商业产品。Chol的加⼊可以促进脂链的堆积和双分⼦层的形成,调节膜的流动性/刚性,并进⼀步影响药物释放、脂质体的稳定性和胞外分泌动⼒学。对于Shingrix(带状疱疹疫苗,含有糖蛋⽩E抗原和AS01B脂质体佐剂系统)的产物,Chol可以避免QS21(AS01B佐剂系统中的免疫增强剂之⼀)以2:1的⽐例(Chol:QS21,w/w)⽔解。对于AmBisome的产物,与⾮甾醇相⽐,Chol降低了脂质体制剂的毒性。Chol对双分⼦层性质的影响是浓度依赖性的。据报道,低浓度(2.5mol%)和⾼浓度(>30mol%)的Chol对脂质双分⼦层的性质影响不⼤。5<Cholmol%<30的Chol的“冷凝效应”或“有序效应”导致颗粒⼤⼩从220nm逐渐增⼤到472nm,膜的流动性降低,药物释放减少。除了Chol,其他与Chol结构相似的甾醇,如⻩体酮、⻨⻆甾醇和⽺⽑甾醇,也被研究⽤于调节膜的刚性和稳定性。一些常用于标记脂质体的荧光染料包括:DiO、DiI、Rhodamine PE、NBD、BODIPY、Cy3和Cy5等。
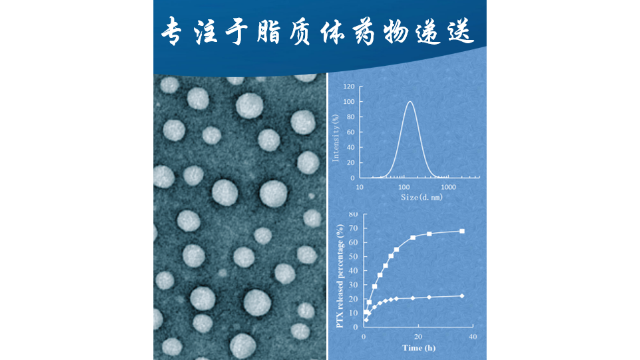
载药脂质体如何纯化如果需要纯化载药脂质体,通常会根据载药脂质体的性质和所需纯度要求选择合适的纯化方法。以下是一些可能的纯化方法:1.超滤法:超滤可以用于去除较大的杂质和未包埋的药物。通过选择适当的分子量截止膜,将载药脂质体溶液经过超滤膜,较大的杂质和未包埋的药物将被截留,而较小的载药脂质体颗粒则通过膜孔。2.凝胶过滤法:凝胶过滤可以利用凝胶材料的孔隙大小分离分子。将载药脂质体溶液加入到凝胶柱中,通过洗脱的方式,较小的载药脂质体颗粒会通过凝胶柱,而较大的杂质则会被截留在柱中。3.离心法:离心可以将载药脂质体颗粒沉淀到底部,去除上清液中的杂质和未包埋的药物。将载药脂质体溶液进行高速离心,使载药脂质体颗粒沉淀到离心管底部,然后去除上清液中的杂质和未包埋的药物。4.柱层析法:柱层析可以利用吸附剂对溶液中分子的亲和性分离。将载药脂质体溶液通过填充有吸附剂的柱子,通过洗脱的方式,使载药脂质体颗粒和杂质分离出来。5.其他方法:根据具体情况,还可以考虑其他纯化方法,如凝胶电泳法等。选择合适的纯化方法需要考虑载药脂质体的性质、所需纯度要求以及纯化效率等因素。通常会结合多种方法进行纯化,以达到所需的纯度和纯净度。脂质体各组分对核酸递送效率的影响。内蒙古北京脂质体载药
阳离子脂质体提高siRNA的细胞递送和基因沉默效率。内蒙古北京脂质体载药
固体脂质纳米颗粒和纳米结构脂质载体虽然脂质体作为药物载体是有用的,但它们需要使用有机溶剂的复杂生产方法,在包裹药物方面表现出低效率,并且难以大规模执行。固体脂质纳米颗粒(SLN)和纳米结构脂质载体(NLC)的开发是为了解决这些缺点。传统的脂质体由液晶脂质双层组成,而SLN由固体脂质组成,和NLC由固体和液晶脂质混合物组成。SLN和NLC的粒径在40~1000nm之间。SLN和NLC表现出增强的物理稳定性,解决了脂质体基础配方的主要限制之一。SLN和NLC还具有更高的装载能力和更高的生物利用度,不需要使用有机溶剂就可以大规模生产,并且比其他LNPs更稳定。此外,分子在固体状态下迁移率的降低使得SLN和NLC能够更精确地控制其药物有效载荷的释放。然而,在长期储存中,SLN的结晶可以将掺入的药物排出到周围介质中内蒙古北京脂质体载药