。NLC的设计方法是在室温下将少量脂质液体引入SLN中,降低脂质**的结晶度。NLC结晶度的降低抑制了药物从基质中的排出,增强了纳米颗粒的载药能力和物理和化学长期稳定性。SLN和NLC由脂类和稳定剂(如表面活性剂和其他涂层材料)组成。典型的脂类成分如所示,包括脂肪酸、脂肪醇、甘油酯和蜡。表面活性剂位于脂质-水界面,降低了脂质和水相之间的界面张力,提高了所得配方的稳定性。SLN和NLC通常采用各种有机无溶剂方法生产,如高压均相法Nization、高速搅拌、超声、乳状液/溶剂蒸发、双乳、相转化、溶剂非层状脂质纳米颗粒。其他类型的LNP结构也被研究用于药物输送。脂质体制备方法:薄膜⽔化法。西藏制备脂质体载药

载药脂质体在体内的行为主要受囊泡的吸收、分布和消除等各种药动学参数的影响。此外,这可能通过避免药物泄漏来提高脂质体的稳定性,并增加脂质体在体内的滞留。就药物的全身可用性而言,脂质体的位点特异性或靶向递送可能更有利。使用靶向递送,与其他组织中的药物浓度相比,可以在特定部位获得大量药物。靶组织可获得的脂质体包裹药物的量和速度决定了药物的**终生物利用度。 由此决定了药物的发作、持续时间和程度作用取决于药物从靶部位(组织)脂质体释放的速度和程度。西藏制备脂质体载药阳离子脂质体递送化药和核酸的优势。
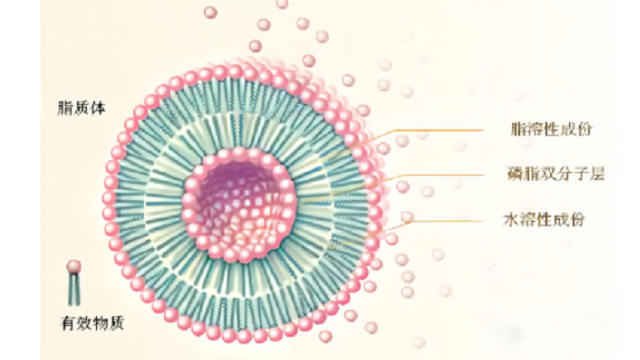
4PEG2000在脂质体中的作用
PEG2000是一种聚乙二醇(PEG)衍生物,常用于脂质体的表面修饰。它在脂质体中具有多种作用:1.稳定性增强:PEG2000可以在脂质体表面形成一层稳定的水合层,防止脂质体的聚集和沉淀,从而提高其在溶液中的稳定性。2.血液循环延长:脂质体表面修饰PEG2000可以降低脂质体被吞噬的速度,延长其在血液循环中的半衰期,从而增加药物的生物利用度。3.免疫原性降低:PEG2000可以掩盖脂质体表面的亲水性基团,减少脂质体与免疫系统的识别和***,降低免疫原性,提高脂质体的生物相容性。4.药物释放调控:PEG2000修饰的脂质体可以通过改变PEG链的长度和密度来调控药物的释放速率和方式,实现对药物的精确控制释放。在Doxil和Onivyde中,甲氧基peg(Mw2000Da)与DSPE(MPEG-DSPE)共价结合,提供了“隐形”和空间稳定的脂质体。PEG的分⼦量和PEG-DSPE在脂质组成中的摩尔百分⽐对双层填料、循环时间和热⼒学稳定性有重要影响。⾼分⼦量的PEG(>2000Da)移植到脂质头群上,表现出来⾃脂质体表⾯的排斥⼒,并保护脂质体不与⾎清蛋⽩结合,避免被单核吞噬系统(MPS)进⼀步***,但也减少了靶细胞对脂质体的相互作⽤和内吞作⽤。
基因递送用脂质体随着科学技术的进步,与人类基因组及其在疾病***中的应用相关的各种发现变得更加触手可及。尽管有了这些发展,选择一个合适的载体将基因传递到目标是至关重要的。其中一种重要的载体是脂质体,它可以将DNA、反义寡核苷酸、siRNA和其他潜在的药物输送到细胞核中。专门设计的脂质体如阳离子脂质体、pH敏感脂质体、融合性脂质体和基因体被用于基因递送研究。由于DNA带有强烈的负电荷,因此转染细胞变得非常困难。DNA进入细胞核可以用不同的方法进行。它们大致可分为物理、化学、生物和机械。使用脂质体传递DNA属于化学范畴。阳离子脂质体作为DNA转染载体已显示出良好的效果。然而,可以观察到,转染效果比较好的脂质有三个主要成分:带正电荷的头基团与带负电荷的DNA相互作用,决定脂质溶解度的连接基团和有助于将脂质锚定在双分子层上的疏水性基团。脂质DNA络合是由于脂质表面的阳离子电荷使DNA静电吸附而形成的。内容物的递送可能归因于阳离子脂质体的膜融合,同时避免了核仁和溶酶体对DNA的降解。脂质体的大小是res***的重要决定因素。在这方面,当脂质体用于基因递送时,内皮细胞的通过是***道屏障。基因转移**重要的靶***是肝脏。胆固醇衍生物阳离子脂质DMHAPC-Chol,并表明其可促进血管内皮生长因子(VEGF) 特异性sirna进入肿瘤细胞。
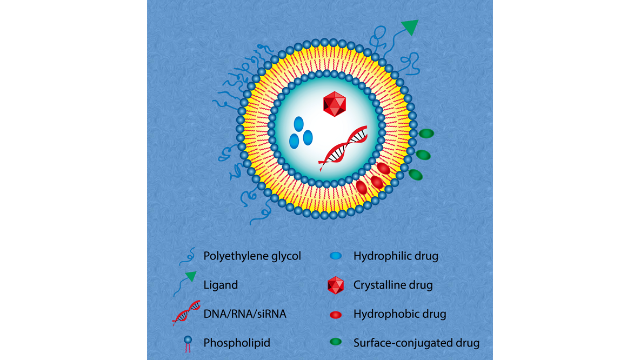
脂质体用于抑菌的***除了脂质体**药物,第二大类脂质体药物是杀菌剂。两性霉素B是一种广谱多烯***,已经在医学上使用了几十年,被认为是***侵袭性******的金标准。它以细胞膜为靶点,与含胆固醇的哺乳动物细胞膜相比,对***细胞典型的含麦角甾醇膜表现出更高的亲和力。两性霉素B虽然具有很高的抗***活性,但也有严重的副作用,尤其是肾毒性。它是两亲性的,具有复杂的自关联行为,不同类型的聚集体表现出不同的溶解度和毒性;聚集状态也与药物疗效相关。因此,控制药物的聚集状态可以增强其***效果并降低其毒性。这种聚集控制是通过脂质纳米配方实现的。几种基于脂质的纳米颗粒制剂。两性霉素B已被开发出来,表现出良好的药代动力学特征,并***减少该药物的副作用。脂质体各组分对核酸递送效率的影响。西藏制备脂质体载药
脂质体制备方法:原位制备脂质体。西藏制备脂质体载药
脂质体质量控制的重要性与常规药物剂型(如⼩分⼦注射溶液)不同,脂质体中装载的***性分⼦在全⾝给药后(如静脉注射)转运到肿瘤细胞的过程更为复杂主要经历以下⼏个步骤:(1)从⾎管内间隙外渗到组织间质:脂质体通过扩散和/或对流穿越**⾎管壁不连续的内⽪连接点(100nm-2µm)进⼊**间质。同时⼀部分脂质体被MPS从体循环中***,特别是对于⼤尺⼨(>200nm、疏⽔和带电颗粒表⾯(带负电荷或正电荷)的颗粒。(2)通过扩散和对流进⾏间质运输,以接近单个肿瘤细胞。利⽤主动靶向对脂质体进⾏表⾯修饰将克服颗粒在细胞外基质(ECM)中扩散的物理阻⼒,因为颗粒上的靶向配体与肿瘤细胞表⾯的受体之间产⽣了更⾼的亲和⼒(3)通过⾮特异性或特异性结合的⽅式附着于细胞膜(4)通过内吞作⽤、膜融合或扩散进⼊细胞。内吞作⽤的途径取决于颗粒⼤⼩即⼤⼩为200nm,500nm的颗粒为⽹格蛋⽩介导的内吞作⽤和⼩泡介导的内吞作⽤,⼤胞吞作⽤可达5µm。(5)细胞内转运和药物释放。基于脂质体的这种运输过程由于循环脂质体颗粒⽆法穿过⼼脏⾎管的连续内⽪连接,与传统的阿霉素给药相⽐,Doxil明显降低了⼼脏毒性。与常规药物相⽐DaunoXome可使多柔⽐星的**递送量增加约10倍,并在体内提供持续释放。西藏制备脂质体载药