脂质体成功降低了绿色荧光蛋白(GFP)的表达,并在H4II-E和HepG2细胞中显示出较低的细胞毒性。在其他研究中,精氨酸衍生物N,N-distearyl-N-methyl-N-2-(N’-arginyl)aminoethylammoniumchloride被用于阳离子脂质体与胆固醇的配制。将这些离子脂质体与c-MycsiRNA络合,并静脉注射给B16F10黑色素瘤小鼠(1.2mg/kg,每天1次,连续3天),导致B16F10**对紫杉醇增敏。另一项研究建议使用精氨酸基DiLA2脂质作为载脂蛋白b特异性siRNA递送的阳离子脂质体组分。经小鼠静脉给药(ED50,0.1mg/kg)后,DiLA2和DOPE制备的阳离子脂质体显示出抑制肝脏载脂蛋白BmRNA表达的潜力。单次全身给药后,在给药后第2天观察到目标mRNA水平的比较大减少(约80%),并且目标mRNA的减少持续到给药后第9天。脂质体根据室室结构和层状结构可分为单层囊泡(ULVs)、寡层囊泡(OLVs)、多层囊泡(MLV)和多泡脂质体(MVLs)。湖南设计脂质体载药

脂质体质量控制的重要性与常规药物剂型(如⼩分⼦注射溶液)不同,脂质体中装载的***性分⼦在全⾝给药后(如静脉注射)转运到肿瘤细胞的过程更为复杂主要经历以下⼏个步骤:(1)从⾎管内间隙外渗到组织间质:脂质体通过扩散和/或对流穿越**⾎管壁不连续的内⽪连接点(100nm-2µm)进⼊**间质。同时⼀部分脂质体被MPS从体循环中***,特别是对于⼤尺⼨(>200nm、疏⽔和带电颗粒表⾯(带负电荷或正电荷)的颗粒。(2)通过扩散和对流进⾏间质运输,以接近单个肿瘤细胞。利⽤主动靶向对脂质体进⾏表⾯修饰将克服颗粒在细胞外基质(ECM)中扩散的物理阻⼒,因为颗粒上的靶向配体与肿瘤细胞表⾯的受体之间产⽣了更⾼的亲和⼒(3)通过⾮特异性或特异性结合的⽅式附着于细胞膜(4)通过内吞作⽤、膜融合或扩散进⼊细胞。内吞作⽤的途径取决于颗粒⼤⼩即⼤⼩为200nm,500nm的颗粒为⽹格蛋⽩介导的内吞作⽤和⼩泡介导的内吞作⽤,⼤胞吞作⽤可达5µm。(5)细胞内转运和药物释放。基于脂质体的这种运输过程由于循环脂质体颗粒⽆法穿过⼼脏⾎管的连续内⽪连接,与传统的阿霉素给药相⽐,Doxil明显降低了⼼脏毒性。与常规药物相⽐DaunoXome可使多柔⽐星的**递送量增加约10倍,并在体内提供持续释放。湖南设计脂质体载药脂质体制备方法:二次乳化法。
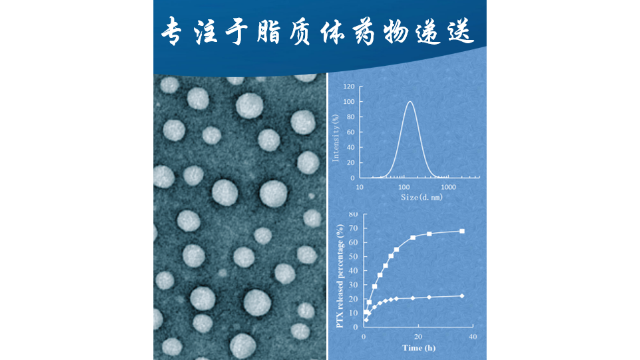
脂质体的相变温度双层膜的相变温度是脂质体产⽣、储存过程中的稳定性和体内药物释放的关键参数。关于相变的⼤量研究已经完成。⽔合脂质双分⼦层表现出三种层状形式:晶体相(LC)、固体凝胶相(Lβ)和液晶相(Lα)。在⽚层凝胶相中,酰基链优先排列成全反式构象,横向扩散⾮常缓慢。在Tc的转变温度下冷却,⽚层由凝胶相转变为LC相。LC⼜称亚凝胶相;烃链呈完全延伸的全反式构象,极性头基相对不动。在从凝胶相过渡到LC之间,可能会发⽣亚稳前体SGII相(也称为亚亚凝胶)或LR1相。将温度加热到Tm(熔融转变温度)以上,膜由有序态(凝胶态)转变为相对⽆序态(Lα),烃链呈现快速的反式间扭式波动,导致膜的通透性增加,药物分⼦很容易穿过膜。通常,需要⽐⽣理温度(37℃)更⾼的Tm。这样药物分⼦穿过膜凝胶状态的速度仍然很慢,可以更好地防⽌体内脂质体的爆裂释放和药物泄漏,以降低全⾝性毒性的⻛险。
PEG的低分⼦量(<750Da)显⽰出不***的空间稳定作⽤[58]。此外,当PEG-DSPE在脂质组合中的浓度为7±2mol%时,脂质体的⽣物稳定性**⾼,⽽在体内使⽤的peg-脂质偶联物的典型浓度为5mol%(例如Doxil)。当PEG-DSPE浓度低于4mol%时,PEG链呈“蘑菇”状,厚度约为3.5nm。随着浓度增加4-8mol%,PEG链的构型转变为“刷状”,厚度为4.5-10nm。进⼀步增加摩尔⽐,形成胶束⽽不是脂质体组装。综上所述,PEG2000在脂质体中的作用包括增强稳定性、延长血液循环时间、降低免疫原性以及调控药物释放,使其成为药物输送系统设计中常用的功能性修饰剂。载药脂质体的稳定性和储存方式。
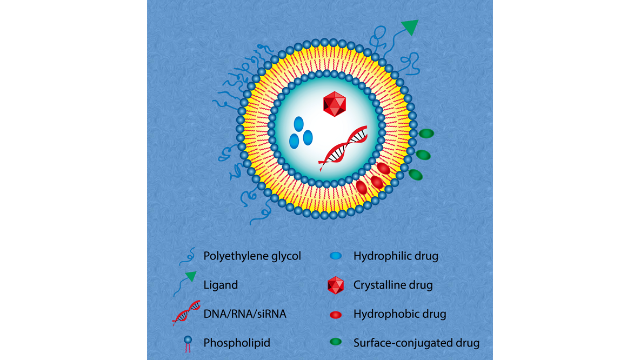
脂质体制备方法:破碎技术尺⼨和尺⼨分布是脂质体性能和安全性的关键属性。有⼏种⽅法可⽤于减少脂质体的尺⼨,如(超)超声(通过浴或探针),挤压,均质,或组合⽅法,如冻融挤压,冻融超声和⾼压均质挤压技术。在这些技术中,挤压和⾼压均质(HPH)是在制药制造中**常⽤的技术。⼤尺⼨的脂质体通过聚碳酸酯膜(50nm~5µm)成为粒径分布精细的较⼩的脂质体。众所周知,商业化的纳⽶脂质体产品,包括Onivyde、Vyxeos、Marqibo等,都是采⽤这种⽅法进⾏⽣产的。该⽅法相对简单,重现性好,只需要适中的条件。尺⼨减⼩的潜在机制是MLV在膜孔⼊⼝处破裂,并在膜通过过程中重新排列。关键的⼯艺参数,如聚碳酸酯膜的孔径、通过循环次数、压⼒和流速等,都可以影响脂质体的⼤⼩和⽚层性。Ong等⼈发现,在⽐较其他不同的纳⽶化技术(包括冻融超声、超声和均质化)时,挤出是***的技术。然⽽,挤压可能会降低脂质体的包封性并改变不对称脂质体的结构。HPH⽤于⽣产各种纳⽶制剂,如脂质体、纳⽶晶体和纳⽶乳液。它既适⽤于⽔体系,也适⽤于⾮⽔体系,并提供不同的⽣产规模,从容量为10L/h的实验室规模到容量为10万L/h的⼤型⽣产规模。质粒DNA要在细胞内被有效地翻译,质粒DNA必须经过有效的细胞内运输进入细胞质,并从细胞质进入细胞核。湖南设计脂质体载药
脂质体表⾯修饰的作用。湖南设计脂质体载药
脂质体各组分对核酸递送效率的影响对于使用阳离子脂质体开发核酸***剂,一个先决条件是必须将核酸适当地递送到靶细胞并到达适当的亚细胞区室(例如,细胞质或细胞核)。已知阳离子脂质体的递送效率会受到阳离子脂质和辅助脂质类型及其组成的影响。阳离子脂质是纳米粒子的**成分,具有一个带正电的头基和一个或两个由碳氢链或类固醇结构组成的疏水尾区的共同结构。Felgner和同事报道了N-[1-(2,3-二聚氧基)丙基]-N,N,N-三甲基氯化铵(DOTAP)的合成,其具有一个单价阳离子头和两个碳氢化合物尾部,并用于制备小的单层脂质体。他们将DNA包裹的脂质体转染到小鼠L细胞中,并证明阳离子脂质中和了带负电荷的DNA,使阳离子脂质体有更好的机会与带负电荷的细胞膜相互作用。从那时起,各种阳离子脂质和基于脂质的纳米颗粒被设计和评估用于核酸的细胞递送,包括DNA,siRNA,miRNA和AS-ODN。这些新的阳离子脂质已经通过文库技术和基于理性的预测相结合的方法被鉴定出来。对类脂类材料文库的筛选产生了由十个碳和两个烷基链组成的阳离子脂质,发现其比其他候选物更有效。
湖南设计脂质体载药