静置25分钟后把酒精倒干,用吸水纸吸出多余的酒精,然后配压缩胶,同样的操作,关键是梳子要插得快,要小心梳子下产生气泡,然后静置30分钟。如果是当天跑胶,我会等上层胶凝2个小时再用,但要注意防干燥缩水,可以在一个小时的时候沿着梳子上缘加点电泳液。所以我一般提前一晚制胶,泡于纯水或者电泳液里置于4度冰箱暂存。三、蛋白电泳1、上样前准备把胶组装到电泳芯上,注意密闭性(否则漏液),如果内槽漏液就不是匀强电场了,条带可能就不是一条直线。然后内槽倒满电泳液,拔梳子,这一步要小心,梳子要两边一起缓缓往上拔出,然后观察泳道内有无脱落的胶粒或者胶丝,有的话用1毫升注射器吸出。然后从冰箱取出蛋白样品,解冻。准备振荡器。2、上样和电泳注意,上样后蛋白会开始慢慢在胶中弥散,所以上样越快越好。我习惯先上蛋白Marker,再上蛋白样品,蛋白上样前确保样品完全解冻和充分振荡(推荐使用振荡器振荡),吸的时候没有拉丝即可,建议上样分钟把样品从冰上取出来,不然样品中SDS可能会结晶析出,从而影响电泳效果。上层胶80V25分钟,下层胶120V65分钟。四、转膜1、转膜前准备我会在电泳结束0分钟准备,把转膜液配好置于4度冰箱预冷,然后裁膜,准备转膜装置。科研中我们涉及到的免疫沉淀实验通常指:免疫共沉淀(Co-IP)、RIP、Chip等等,将几种实验简单概述一下。豚鼠科研技术服务构建
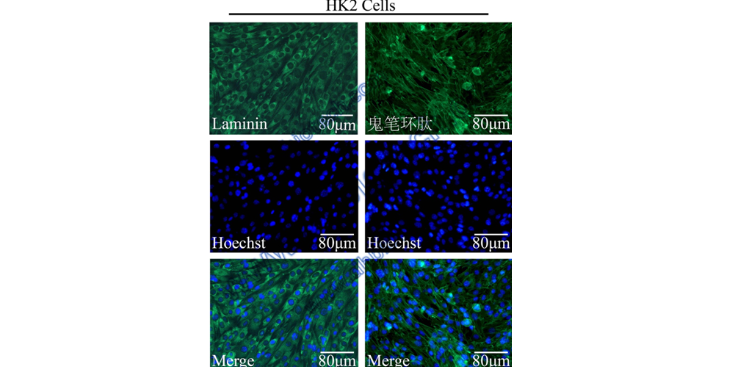
3)基因/蛋白质表达定性或定量检测在进行分子检测的过程中,保持核酸和蛋白质的完整性至关重要,因此在取样过程中,应尽量避免核酸及蛋白质的降解。如不注意采样过程,将会导致样本中的核酸及蛋白质的无差别降解,严重影响后续分子检测结果。在条件允许的情况下,样本在离体后应立刻装入冻存管内,并立即放入液氮中进行冷冻。在RNA提取样本的保存过程中,可以选择非冷冻型RNA保存液或Trizol试剂进行RNA酶的。针对蛋白质提取样本的保存,我们同样可以使用商品化的蛋白酶剂进行短期处理。聚合酶链式反应(PolymeraseChnReaction,PCR)及免印迹(Westernblotting,WB),这两种实验手段是分子学检测中不可或缺的一部分,也是发表至关重要的分子检测数据。PCR主要用来对基因在基因组层面或转录层面的变化进行定性或定量检测,而WB则主要用来对某一蛋白质的表达进行定量检测。(4)转录组学、蛋白质组学及代谢组学检测随着检测水平及相关产业的不断发展,各类组学检测的价格降低,实验设计中也常常运用组学检测来提升实验设计的档次。在我们进行转录组学及蛋白质组学的检测过程中,同样是要首先确保目标RNA或蛋白质的片段完整性。豚鼠科研技术服务构建科研技术服务致力于推动前沿科技的研究与发展,为企业提供定制化的技术解决方案。
1.首要原则:细胞不重要情况下立即丢弃,培养箱灭菌,所用培养基也都要丢弃,器械等重新灭菌或拆用新的。2.细菌污染一般都救不回来了,发现的时候培养基一般都很浑浊且细胞都死了3.污染且细胞很重要时:遇到念球菌污染,且细胞为基因改造细胞,非常重要。如231贴壁乳腺细胞,发现细胞周围出现很小的串珠透亮圆点,非常像念球菌污染,此时细胞状态尚可,且污染少。处理如下:用预热或室温PBS清洗3次,可适当振摇,将污染冲洗下来。随后加入10-20%双抗到培养瓶,置于37度培养箱1h,之后再用PBS清洗三遍,直至视野下无可见污染。此时细胞也被冲下大部分,因此此方法只适用在细胞贴壁强,状态好,密度高时使用。之后每天再更换培养基,每次用PBS冲洗2遍。过几天细胞状态尚可时,消化离心时用500r,3min,去掉上清,重复3次。这个方法是根据文献可利用念球菌和细胞体积重量差异实现分离。基本上这一步做完以后,污染就基本了,接下来就注意多观察,勤换液就行。
外泌体的功能外泌体可能作为细胞之间物质和信号通讯的途径,不同的细胞通过分泌携带不同组分的外泌体实现细胞间通讯,这些外泌体被受体细胞吸收,通过物质交换或释放内含物实现物质和信号的交流。外泌体与受体细胞的信息交流可能通过以下4种途径实现:外泌体表面膜蛋白质被目的细胞表面的受体识别,从而靶细胞;外泌体在蛋白酶作用下产生的表面膜蛋白质碎片可作为目的细胞表面受体的配体;外泌体脂膜可以与目的细胞膜融合,将蛋白质和RNA等内容物释放进去,此类膜融合可能改变靶细胞的一些膜特性,例如脂质和膜蛋白质的密度及种类;目的细胞通过胞吞的形式摄入外泌体经由以上几种途径,外泌体将其携带的生物信息运输到周边靶细胞或经血液等体液运输而被远处组织细胞摄取,进而影响目的细胞的基本功能和基因表达。几乎所有的细胞都可以在自发或在一定刺激条件下产生外泌体,不同的细胞产生的外泌体具有不同的功能,这些外泌体参与了一系列生理和病理过程,如发生与发展、抗原呈递、免疫调节、组织愈合等。此外,外泌体与疾病的研究表明:外泌体可能在代谢性疾病的出现以及心血管健康中发挥作用。通过不同分组之间的细胞对于划痕区修复能力的不同,可以判断各组细胞的迁移与修复能力的差别。
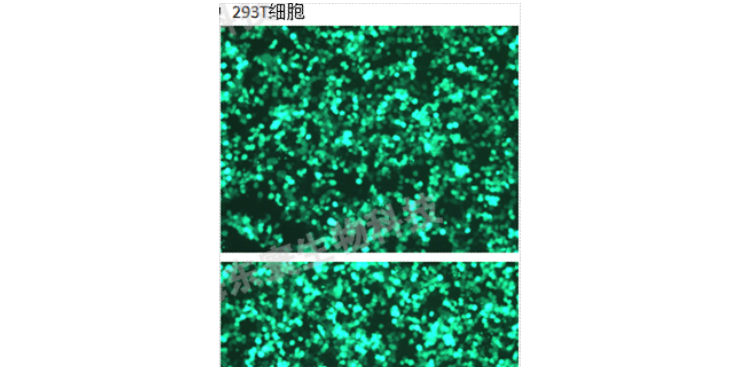
m6A研究又有新手段了?赶紧来了解一下吧!栏目:研究动态发布时间:2019-08-14RNA甲基化m6A是如今的研究热点之一,Cell上新发表了一篇介绍不使用m6A抗体的检测mRNAm6A水平的Resource文章......RNA甲基化m6A是如今的研究热点之一,目前主要的研究思路包括差异表达的write,reader和eraser基因分析;m6A抗体检测全转录组甲基化水平;分析m6A甲基化水平变化的靶基因和下游机制研究。而在7月25日的Cell上新发表了一篇介绍不使用m6A抗体的检测mRNAm6A水平的Resource文章,小编时间和大家分享一下。作者开发这一方法的前提是有研究报道了MazF能特异性的识别无修饰的ACA序列并发挥RNA酶活性在ACA之前剪切底物。但ACA序列的个A发生m6A甲基化之后将无法被MazF所识别,如图一所示。图1MazFRNA酶作用示意图根据这一原理,作者将纯化后的mRNA进行MazF酶处理,然后再对打断的RNA进行逆转建库测序。对于无修饰的位点,ACA处被完全剪切,测序reads正好分布于该位点上下游而且比对至该处的上下游reads数是相同的.如图2所示。而甲基化位点的reads会包含上下游的序列。作者开发了MAZTER-MINE软件包专门进行分析(图3)。protocol 分享|小鼠卵巢组织切片 HE 染色。湖南动物科研技术服务构建
随着科技的不断进步,科研人员将能够开发出更为精确、实用的动物模型,更好地为人类健康保驾护航。豚鼠科研技术服务构建
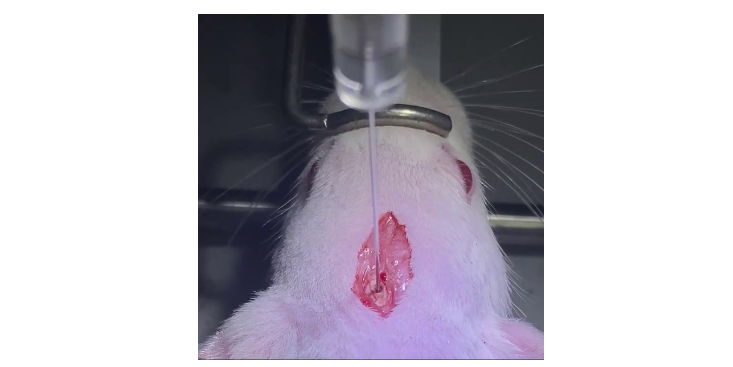
我们知道WB实验步骤繁琐,一次实验历时也不短,从提蛋白到显影结束可能要三天,我们就讲一下这里面的一些关键环节。一、蛋白提取及变性1、提取蛋白很多经验丰富的WB实验者都深有体会,蛋白提取是影响结重要的环节之一。该过程重要的是防降解和保证蛋白浓度不要太低。防降解主要有两点,一是裂解前注意保持样品处于低温环境中,二是裂解时加入足够的蛋白酶抑制剂。我们习惯先用冰冷的PBS做心脏的体循环灌注,然后冰上取脑,分离各脑区(嗅球,皮层,海马,中脑,小脑,延髓,丘脑,纹状体)后置于,用液氮速冻后转移至-80度冰箱长期保存。接着是保证蛋白浓度,即要加入适量的裂解液,加太少会使蛋白提取不充分,加太多会让蛋白浓度太低,一般经验是这样的,细胞样品例如一个六孔板的细胞加60微升的裂解液,动物组织的话每毫克组织加10微升裂解液。还要加上超声破碎处理,具体方案见讨论部分。如果没有超声破碎仪,那就用1毫升注射器不断抽吸,冰上反复抽吸1分钟左右,注意不要产生过多气泡。(需要灌注取材的视频可以私聊获取,由于文件过大,又比较血腥,不宜直接放到文章里。)2、蛋白变性加入上样缓冲液后100摄氏度煮10分钟,这里的上样缓冲液有两种可选。豚鼠科研技术服务构建