- 品牌
- 同顺生物
在成像应用中,D-荧光素钾盐的生物相容性与代谢动力学特性成为其性能优势的关键体现。该化合物易溶于水(溶解度达30mg/mL),可通过腹腔注射(150mg/kg)、静脉注射(10μL/g体重)或鼻内给药(50μL,3mg/mL)等多种方式进入生物体。注射后10-15分钟,光信号达到峰值平台期,此时体内分布均匀且信号强度与荧光素酶表达量呈线性正相关。以疾病模型研究为例,将携带荧光素酶基因(Luc)的疾病细胞植入小鼠体内后,定期注射D-荧光素钾盐可通过生物发光成像系统(BLI)实时监测疾病生长与转移。实验数据显示,腹腔注射150mg/kg剂量下,小鼠体内光信号半衰期约为20分钟,信号衰减率低于0.5%/分钟,确保了长时间成像的稳定性。此外,其代谢产物主要通过肾脏排泄,24小时内尿液中累计排出量超过90%,体内残留极低,避免了长期蓄积对实验结果的干扰。这种快速去除特性也使其在重复给药实验中具有明显优势,在药物疗效动态监测中,可每日进行成像而无需担心底物残留影响。化学发光物三联吡啶钌体系,需严格控制电极电位防止副反应。安徽9-吖啶羧酸
Tris(2,2'-bipyridine)ruthenium(II) hexafluorophosphate,其CAS号为60804-74-2,是一种在电化学发光、光催化以及生物标记等领域有着普遍应用的金属配合物。这种化合物以其独特的结构特性而闻名,中心离子钌(II)与三个2,2'-联吡啶分子配位,形成了高度稳定的八面体结构。在电化学发光方面,它能够在电极表面发生氧化还原反应,生成激发态的钌配合物,随后通过辐射跃迁释放出强烈的光信号,这一特性使得它成为电化学发光传感器中的重要组件,普遍应用于环境监测、食品安全、以及临床诊断等领域。其良好的光催化性能也使其在光解水制氢、环境污染物的光降解等方面展现出巨大潜力。通过调整反应条件和配体结构,科研人员能够进一步优化其光催化效率,为解决能源危机和环境污染问题提供新的思路。常州9-吖啶羧酸化学发光物在智能船舶中用于制作发光船体,提升航行安全。
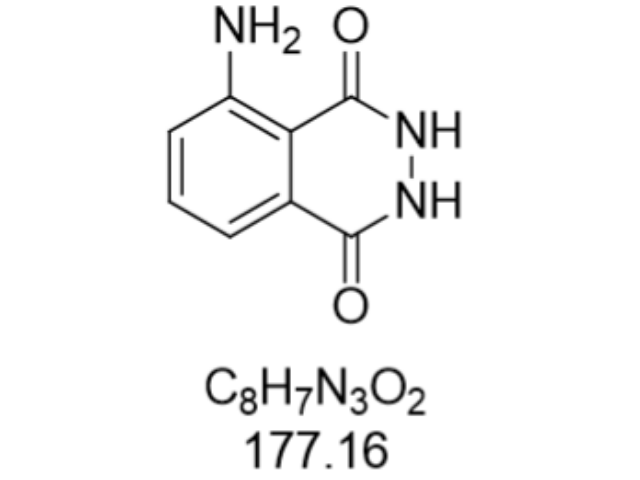
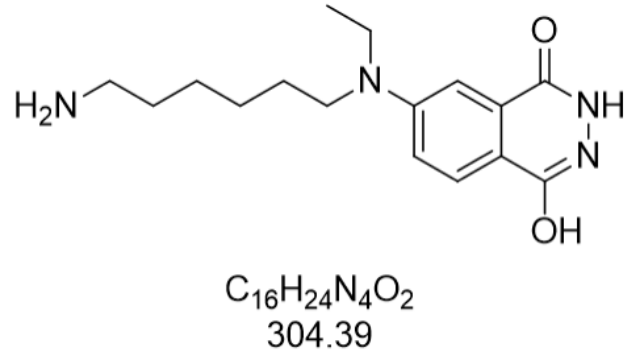
该试剂的偶联性能是其实现分子检测功能的关键技术支撑。AHEI分子末端的氨基基团(-NH2)展现出优异的生物相容性,可与羧基(-COOH)、活性酯(NHS)等官能团通过共价键形成稳定连接。在体外诊断试剂开发中,这种特性使其成为抗体、核酸适体等生物分子的理想标记物。在心肌肌钙蛋白(cTnI)检测试剂盒中,AHEI通过EDC/NHS化学法与单克隆抗体偶联后,形成的免疫复合物在化学发光免疫分析(CLIA)系统中可产生持续30秒以上的稳定光信号,信噪比(S/N)达到12:1以上。更关键的是,其偶联过程在pH 7.4的磷酸盐缓冲液中即可完成,无需极端反应条件,这极大简化了试剂生产工艺。开发的IVD原料级产品,通过优化偶联工艺参数,使单个抗体分子可标记3-5个AHEI分子,在保证检测灵敏度的同时,有效控制了非特异性吸附背景。
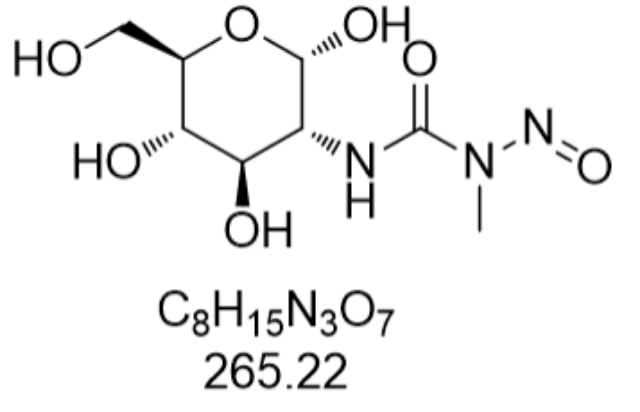
链脲菌素(Streptozotocin,CAS: 18883-66-4)作为一种独特的DNA烷基化试剂,其重要性能体现在对特定细胞类型的高选择性破坏能力上。该化合物通过GLUT2葡萄糖转运蛋白主动进入细胞,这一特性使其对胰岛β细胞及表达GLUT2的神经内分泌疾病细胞具有靶向毒性。实验数据显示,在HL60人类髓系白血病细胞系中,链脲菌素的IC50值只为11.7μg/mL,明显低于四氧嘧啶(ALX)的2809μg/mL,表明其对人类血液系统疾病细胞的杀伤效率是传统烷化剂的240倍以上。这种选择性源于其分子结构中的葡萄糖基部分,该基团模拟天然糖分子被GLUT2转运体识别,而亚硝基脲基团则通过释放甲基正碳离子实现DNA链间交联,导致染色体凝集和细胞凋亡。在动物实验中,单次腹腔注射200mg/kg链脲菌素可使C57BL/6小鼠血糖在72小时内持续高于250mg/dL,成功诱导长久性糖尿病模型,而相同剂量的ALX只造成暂时性血糖波动。化学发光物在药物研发中应用,用于评估药物代谢动力学特征。
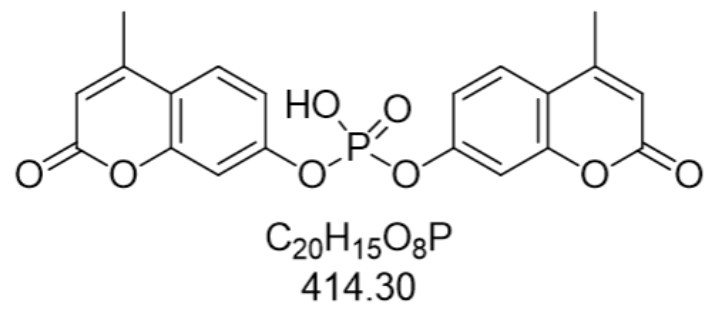
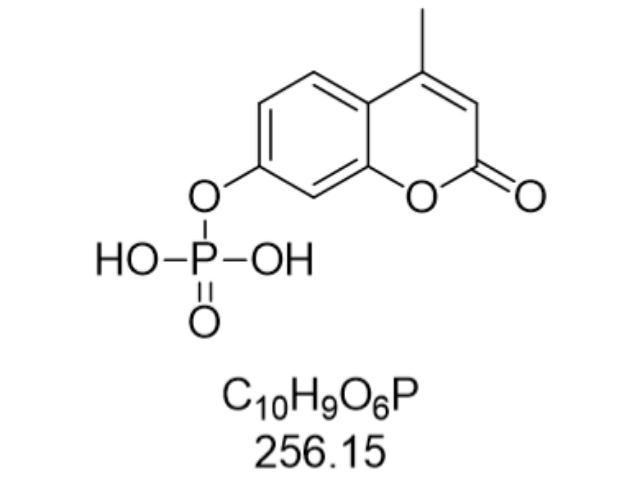
这种结构-性能的关联性使其在碱性条件下能被碱性磷酸酶(ALP)特异性催化水解,生成不稳定的酚氧负离子中间体,随后通过分子内电子转移引发化学发光,发光波长集中在470 nm左右,适用于高灵敏度检测。相较于传统化学发光底物如鲁米诺,AMPPD的背景信号更低,且发光持续时间更长,这得益于其分子内能量传递的高效性以及磷酰氧基水解产物的稳定性。目前,AMPPD已普遍应用于免疫分析、核酸检测及环境监测等领域,尤其在需要低检测限和快速定量的场景中表现出色。化学发光物在法医学中应用普遍,鲁米诺试剂可检测微量血迹痕迹。安徽9-吖啶羧酸
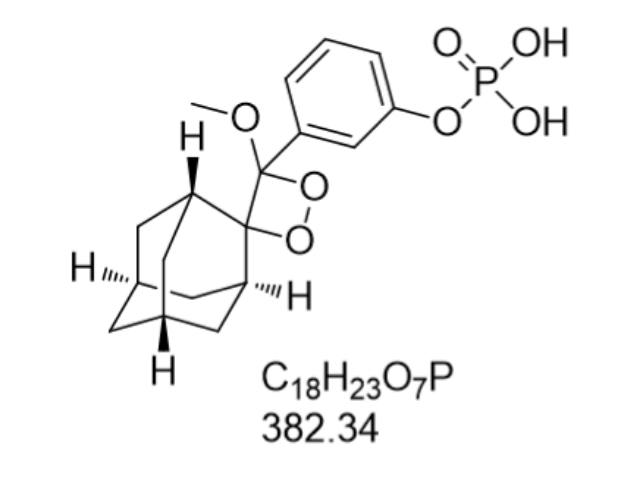
化学发光物金刚烷衍生物,在碱性条件下脱磷酸基团产生光信号。安徽9-吖啶羧酸
腔肠素(Coelenterazine,CAS号:55779-48-1)作为自然界中普遍存在的天然荧光素,其重要性能体现在生物发光体系的构建能力上。该物质化学式为C₂₆H₂₁N₃O₃,分子量423.46 g/mol,是海肾荧光素酶(Rluc)、Gaussia荧光素酶(Gluc)及水母发光蛋白(aequorin)等光蛋白的特异性底物。其发光机制通过氧化反应实现:在分子氧存在下,腔肠素被荧光素酶催化生成高能中间体,释放能量时发射波长集中在450-480 nm的蓝光。这一过程无需三磷酸腺苷(ATP)参与,与萤火虫荧光素酶系统形成明显差异,使其更适用于体内生物荧光研究。在成像中,腔肠素作为底物可实时监测疾病模型中基因表达的变化,其信号强度与细胞内荧光素酶浓度呈线性相关,且背景噪声极低。此外,腔肠素的氧化反应具有钙依赖性,当与水母发光蛋白结合时,只在钙离子浓度升高时触发发光,这一特性使其成为检测细胞内钙离子动态的理想工具。研究表明,使用腔肠素-水母蛋白复合物监测心肌细胞钙瞬变时,其灵敏度可达纳摩尔级别,远超传统荧光染料。安徽9-吖啶羧酸
从产业发展视角观察,鲁米诺钠盐的市场需求正随技术进步持续扩大。全球主要供应商提供从毫克级到克级的不同包装规格。其中,MedChemExpress的HY-15922A型号产品纯度达99.84%,提供LC/MS、NMR等全套质检报告,确保实验结果可靠性。价格体系呈现梯度分布,10mM*1mL水溶液装售价385元,500mg固体装售价350元,满足不同实验室预算需求。在质量控制领域,该物质作为标准物质被普遍应用于药品检测,其含量测定、杂质检查等参数成为衡量生物制品质量的重要基准。随着单细胞分析、微流控芯片等技术的发展,鲁米诺钠盐的纳米级应用研究正在兴起,通过与量子点、金纳米颗粒复合,可构建超灵敏化学...
- 链脲菌素厂家直销 2026-05-16
- 吖啶酯哪家正规 2026-05-16
- 福州腔肠素 2026-05-16
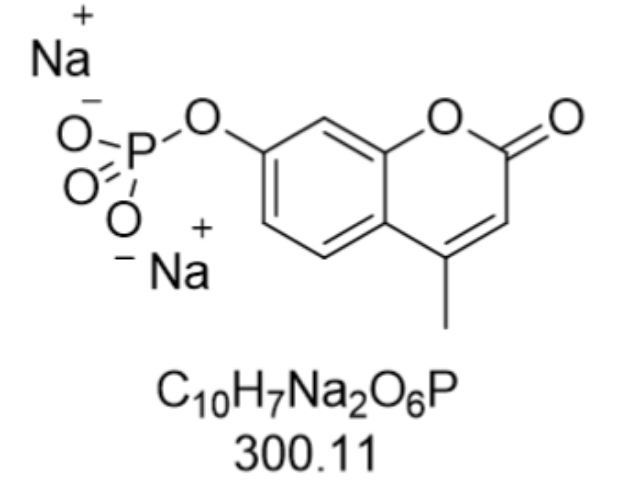
- 双-(4-甲基伞形酮)磷酸酯生产厂家 2026-05-15
- 双-(4-甲基伞形酮)磷酸酯销售 2026-05-15
- 化学发光物供货商 2026-05-14
- 长沙D-荧光素钾盐 2026-05-13
- 银川D-荧光素钾盐 2026-05-13
- 异鲁米诺哪家正规 2026-05-13
- 安徽9-吖啶羧酸 2026-05-13
- D-荧光素钾盐供应商 2026-05-11
- 4-甲基伞形酮磷酸酯 二钠盐求购 2026-05-10
- 贵阳9-吖啶羧酸 2026-05-10
- 鲁米诺哪家好 2026-05-10
- 鲁米诺钠盐采购 2026-05-09
- 鲁米诺价位 2026-05-09


- 鲁米诺制造商 05-16
- 链脲菌素厂家直销 05-16
- 吖啶酯哪家正规 05-16
- 福州腔肠素 05-16
- 苏州胆固醇硫酸酯钾盐直销 05-16
- 阿维巴坦现货 05-15
- 苏尼替尼售价 05-15
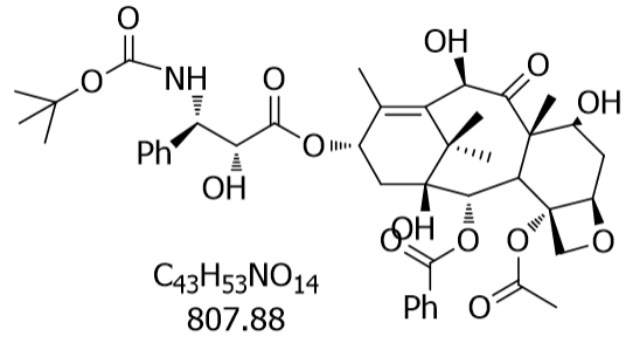
- 乌鲁木齐紫杉醇 05-15
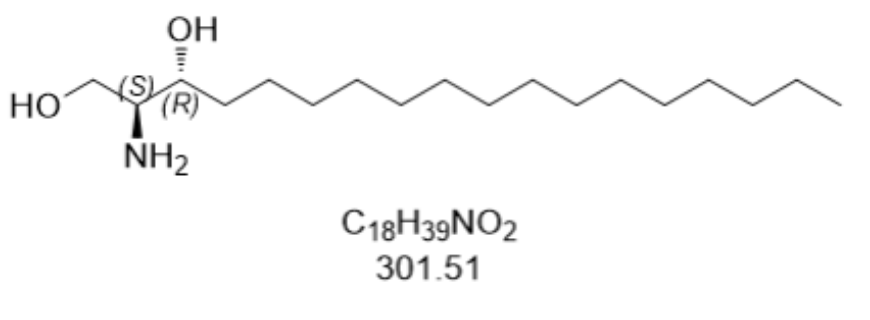
- 二氢(神经)鞘氨醇厂家供货 05-15
- 苏州化妆品添加剂规格 05-15