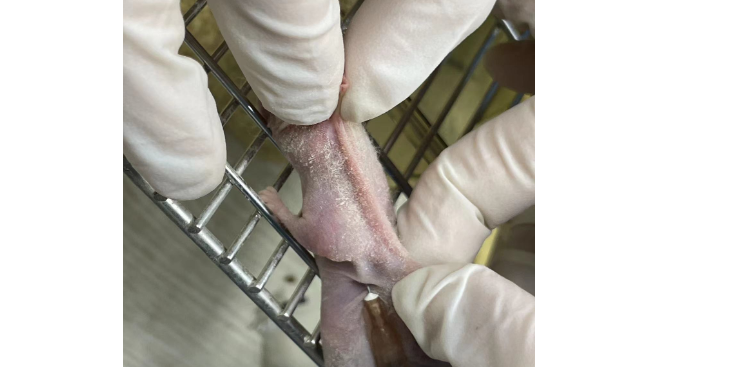
痉挛型脑性瘫痪(SCP)大鼠模型【简介】痉挛性脑瘫指发育异常引起的运动和感觉功能落后,造成肢体肌张力增高、腱反射亢进等一系列综合征。本实验利用脑立体定位解剖图谱,对大鼠的锥体束部位进行精确的立体定位,通过微量注射器对大脑锥体束所在部位注射无水乙醇造成锥体束坏死,的模拟了痉挛型脑瘫的解剖学及病理改变,术后大鼠产生明显的屈曲痉挛症状,且屈肌肌张力增高,症状和体持续时间较长,稳定性良好。从而建立一种可复制性良好且痉挛持续时间较长的稳定的大鼠痉挛型脑瘫动物模型,为进一步深入的探究痉挛型脑瘫的基础研究和临床诊治打下基础【目的】痉挛型脑性瘫痪(SCP)大鼠模型建立【动物】SPF级SD大鼠,雄性,周龄6~8W,体重:200~250g【方法】1、大鼠麻醉,颅顶脱毛备皮;2、大鼠脑定位仪固定大鼠,颅顶正中切口,长度约2cm开口暴露前囟及矢状缝;3、缝线将皮肤左右分开固定,前囟后10mm、矢状缝左侧;4、微量注射器移至开孔处修正骨孔,注射器垂直向颅内插入,缓慢注射无水乙醇15ul,注射完移除注射器,棉球压迫止血;5、缝合创口后维持25°体温,等待苏醒,观察大鼠状态。【观察】术后3天模型大鼠摄食减少、右侧肢体跛行、右前肢不负重、右前肢及右前爪屈曲痉挛明显。免疫系统,人体的免疫系统由免疫细胞、免疫分子构成。组织科研技术服务购买
采用opti-MEM和Lipo3000分别转染含有目的基因的pMSCV-eGFP、VSV、GAG质粒及对照载体,每皿加入脂质体-质粒转染混悬液按购买脂质体相关说明书操作定量。继续培养24h。2)24小时后,将培养基更换为新鲜的DMEM完全培养基,放进细胞培养箱继续培养48~72h。3)48~72h后收集上层培养液,并过μm滤膜,采用ELISA法对所获得的慢载体进行滴度测定。如不及时使用可以冻存于-80℃。3、慢转染1)转染前1天将细胞接种6孔培养板,时细胞的融合率约为50%,前需换液,加入1mLDMEM完全培养基。2)冰浴融化后加入相应体积的液及聚凝胺(Polybrene),混匀后放入37℃孵箱中继续培养3)4h后补充1mL培养基,14h后换液(24h内换液即可)。4)72h后用倒置显微镜观察荧光,监测效率,出现较多荧光时将等量的转染细胞和未转染细胞分别加入等浓度Puromycin(Puromycin或其他筛选浓度需要事先摸索)。5)待未转染细胞全部死亡并且可观察到满意荧光量时,降低Puromycin浓度培养。也可以挑去单克隆细胞株进行进一步培养,以得到满意的稳定表达目的基因的细胞株。6)使用qRT-PCR和Westernblot的方法检测目的基因的表达量和蛋白水平是否显著提高。7)由此可得三组细胞株:a.正常细胞株;b.空载载体的细胞株。贵州组织科研技术服务实验室可以稳定的WB精髓与经验分享。

用一次定量放血法可摆分之摆造成出血性休克,摆分之摆死亡,这就符合可重复性和达到了标准化要求。(三)可靠性复制的动物模型应该力求可靠地反映人类疾病,即可特异地、可靠地反映某种疾病或某种功能、代谢、结构变化,应具备该种疾病的主要症状和体征,经化验或X线照片、心电图、病理切片等证实。若易自发地出现某些相应病变的动物,就不应加以选用,易产生与复制疾病相混淆的疾病者也不宜选用。(四)适用性和可控性供医学实验研究用的动物模型,在复制时,应尽量考虑到今后临床应用和便于控制其疾病的发展,以利于研究的开展。(五)易行性和经济性在复制动物模型时,所采用的方法应尽量做到容易执行和合乎经济条件原则。以上就是上海研录为你分享的小知识,如果想要了解更多相关内容,可与我们联系,我们期待您的来电!
保存于严密紧塞或加盖的容器里,同时在容器外上标签,并随同材料在溶液中投入相应的标签,以免相互混淆。标签上注明固定液、材料来源、日期等。标签上的文字,应用黑色铅笔或绘图黑墨水书写。3.脱水注意事项(1)脱水原理:乙醇与石蜡不相溶,而二甲苯既能溶于乙醇又能溶于石蜡。当组织中全部被二甲苯占有时,光线可以透过,组织呈现出不同程度的透明状态。(2)脱水必须在有盖的玻璃品中进行,防止吸收空气中的水分。(3)在更换高一级的脱水剂时,不要移动材料以免损坏,可用吸管吸出器皿中的脱水剂,再用吸水吸尽器皿内剩余液,然后于皿中加入高一级脱水剂。(4)在低浓度酒精中,每级停留不宜太长,否则易使组织变软,助长材料的解体。(5)在高浓度或纯酒精中,每级停留的时间也不宜太长,否则会使组织变脆,影响切片。(6)如需过夜,应停留在70%酒精中。(7)脱水必须彻底,否则不易透明,甚至使透明剂内出现白色混浊现象。4.透明注意事项(1)使用透明剂时,要随时盖紧盖子,以免空气中的水分进入。(2)更换每级透明剂,动作要迅速,一方面为了不使材料块干涸,另一方面能避免吸收湿气。(3)在透明过程中,如果材料周围出现白色雾状,说明材料中的水未被脱净。建立疾病模型的目的是为了防治人类疾病。
在人类疾病研究中数据表明,常用实验动物模型按产生原因分为以下5类:自发性动物模型、诱发型动物模型、遗传工程动物模型、生物医学动物模型和阴性动物模型。下面上海研录带大家一起看看吧:1、自发性动物模型:是指动物未经任何有意识的人工处理,在自然条件下或基因突变条件下所产生的疾病模型。主要包括突变型的遗传病模型和近郊系的疾病模型。2、诱发型动物模型:亦称实验性动物模型。是使用物理、化学或生物致病因素诱导动物产生某些类似人类疾病表现而制备的动物模型。此模型具有制备方法简单,实验条件容易控制,重复性好等特点,广泛应用于药物筛选、毒理、传染病、病理机制的研究。3、遗传工程动物模型:是利用遗传工程技术对动物基因组进行修饰,用于研究基因功能或疾病机制的动物模型。也称基因修饰动物模型,是指利用胚胎工程和基因工程等生物技术有目的的干预动物的遗传组成,导致动物出现新的性状,并使其能够有效地遗传下去,形成新的可供生命科学研究的和其他目的所用的动物模型。4、生物医学动物模型:也是指利用健康生物的特定生物学特征,研究人类疾病相似表现得模型。这类动物模型与人类疾病存在一定的差异,研究者应加以比较,从中获得有关材料。实验干货 | 分子克隆实验——无缝克隆。海南豚鼠科研技术服务购买
科研技术服务的具体服务内容相当丰富,涵盖了多个方面。组织科研技术服务购买
脓毒症动物模型必须具备以下基本要素:有脓毒症典型的高排低阻血流动力学表现和高代谢状态;伴发多个功能障碍;有较高的自然死亡率,根据脓毒症的转归,要求动物模型的自然死亡率达到50%~70%;脓毒症是严重引起机体的炎症反应过度造成的自身损伤,不是细菌和内对机体的直接损伤,故出现功能障碍及动物死亡距脓毒症模型制备应有一定的时间间距。一般在制模后6~12h后发生的功能障碍或死亡属全身炎症反应所致。实验动物的选择在制作动物模型时多选用雄性小鼠,因为雌性小鼠较雄性小鼠更能耐受脓毒症和失血性休克,且进入发期的雌性小鼠性水平变化很大,而雄性小鼠在脓毒症时更易于发生免疫抑制。为什么选择CLP模型?盲肠结扎穿孔模型(CLP)模型是接近于人类脓毒症机制的模型,被称为脓毒症模型的“金标准”。CLP技术在20世纪70年代被建立。CLP模型非常适宜用于防治脓毒症或脓毒性休克新药的临床前观察造模方法CLP脓毒症模型的建立主要分为两个阶段:盲肠远端结扎和盲肠穿刺。首先是手术引发的结扎部位组织变性坏死引起局部炎症反应,其次是穿孔后使粪便内容物漏入腹膜引起多菌性细菌性腹膜炎,进而诱发全身性炎症反应。组织科研技术服务购买