- 品牌
- 同顺生物
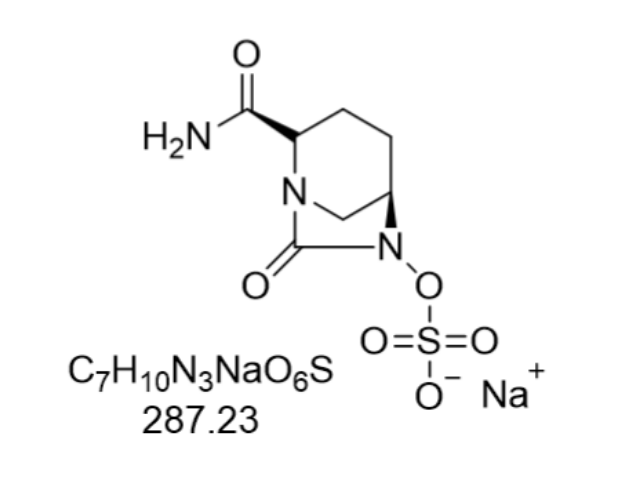
阿维巴坦不仅能够增强头孢的抗细菌效果,还能在一定程度上克服由β-内酰胺酶引起的耐药性,为临床抗被染医治提供了新的选择。阿维巴坦在体外对细胞色素P450酶无明显的抑制作用,表明其与其他药物的相互作用风险较低。尽管阿维巴坦在临床应用中显示出良好的安全性和有效性,但仍需严格掌握适应症和用法用量,以确保患者的用药安全。同时,对于可能存在的细菌耐药机制,如突变性或获得性青霉素结合蛋白外膜通透性降低等,也需密切关注并采取相应的应对措施。原料药国际认证提升企业竞争力。长春艾沙佐咪
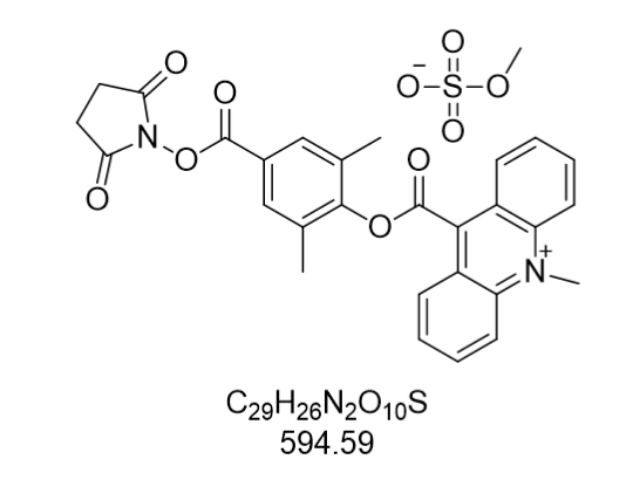
原料药作为医药产业链中的基础环节,其作用至关重要且深远。它们是药物活性的重要组成部分,直接决定了药品的疗效与安全性。在药物研发初期,原料药经过严格筛选与合成,旨在针对特定疾病或症状发挥医治作用。例如,原料药通过抑制细菌生长或杀灭细菌,在医治被染性疾病中扮演着不可或缺的角色;而抗疾病原料药则通过干扰疾病细胞的生长周期或信号传导途径,为患者提供延长生命、提高生活质量的可能。原料药的作用不仅体现在直接的医治效应上,还贯穿于药物制剂的稳定性、生物利用度及给药途径的优化等多个方面,是确保药品质量、实现临床价值的基础。长春艾沙佐咪罕见病用药原料药因需求小众,生产企业需获得政策支持。
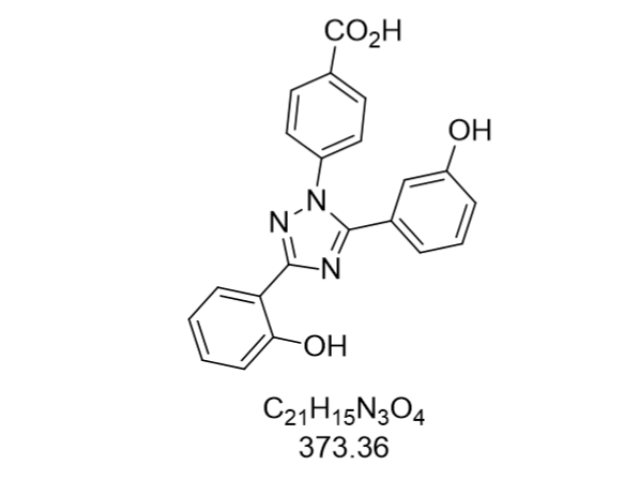
地拉罗司不仅在医治铁过载症方面具有明显疗效,其安全性和耐受性也得到了普遍的认可。作为一种新型的三价铁螯合剂,地拉罗司能够与体内过多的铁离子高度选择性结合,形成可溶性复合物,从而帮助排出多余的铁。这种药物在Ⅱ、Ⅲ期临床试验及药代动力学研究中均表现出了良好的安全性和耐受性。它的使用可以有效控制铁过载,减轻患者的症状。除了主要的医治功能外,地拉罗司还具有一些其他的药物学特性,如抗细菌、抗细胞增殖、抗疟疾和抗氧化应激损伤等。这些特性使得地拉罗司在医治一些其他疾病方面也具有潜力。尽管地拉罗司具有诸多优点,但在使用前仍需告知医生有关自身的过敏史、现有的疾病以及正在服用的其他药物,以确保用药安全。同时,儿童、孕妇、哺乳期妇女以及肝功能受损患者在使用时需要额外谨慎。
诺拉曲特(Nolatrexed),化学式为CAS:147149-76-6,是一种具有明显抗疾病活性的叶酸拮抗剂。它通过干扰细胞内叶酸的代谢过程,特别是抑制胸腺嘧啶合成酶,从而阻断DNA的合成与修复,达到抑制疾病细胞增殖的目的。在临床前研究中,诺拉曲特展现出了对多种实体瘤细胞系的生长抑制作用,为疾病医治提供了新的策略。与传统化疗药物相比,诺拉曲特具有相对较低的毒性,能够减少对患者正常组织的损伤,提高医治的安全性和耐受性。尽管其临床应用尚处于研究和发展阶段,但诺拉曲特所展现出的潜力已经引起了医学界和制药行业的普遍关注。未来,随着对其作用机制的深入研究以及临床试验的推进,诺拉曲特有望成为医治多种恶性疾病的有效药物,为疾病患者带来新的希望。原料药的杂质谱分析助力质量提升。
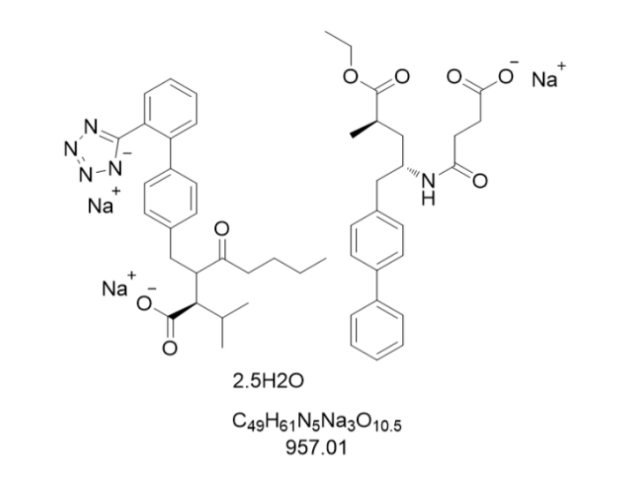
原料药作为医药产业链的重要基础,其质量与供应稳定性直接影响全球药品市场的运行。作为活性的药物成分(API)的直接来源,原料药需经过复杂的化学合成或生物提取工艺,其纯度、杂质控制及晶型结构等参数均需符合严格的药典标准。以某类原料药为例,发酵工艺的微小波动可能导致有效成分含量偏差,进而影响制剂的疗效与安全性。近年来,全球原料药市场呈现明显的区域化特征,中国、印度凭借成本优势和规模化生产能力占据全球60%以上的市场份额,而欧美国家则专注于高附加值技术药原料的研发。这种产业格局下,原料药企业的重要竞争力逐渐从单一的生产能力转向全产业链整合能力,包括上游中间体供应、下游制剂配套以及符合国际标准的GMP管理体系。特别是在危险期间,全球原料药供应链的脆弱性暴露无遗,多国开始推动原料药本土化生产,这一趋势或将重塑未来十年的产业布局。新型原料药研发为医药创新注入活力,前景广阔。长春艾沙佐咪
原料药供应链金融服务可帮助企业缓解资金周转压力。长春艾沙佐咪
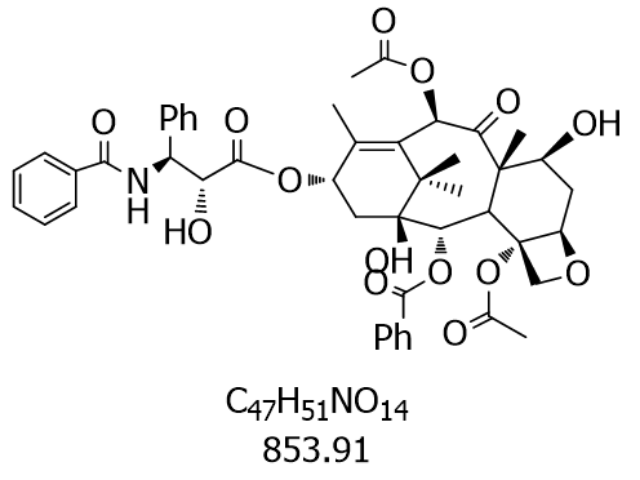
临床应用中,紫杉醇的剂型创新明显提升了疗效与安全性。传统紫杉醇注射液因含聚氧乙烯蓖麻油(Cremophor EL)表面活性剂,易引发严重过敏反应(发生率约40%),需在使用前进行、苯海拉明和西咪替丁的三联预处理。2005年上市的紫杉醇脂质体通过将药物包裹于磷脂双分子层中,降低了过敏风险(发生率降至2%),但制剂稳定性受pH值影响较大。2010年问世的白蛋白结合型紫杉醇(nab-Paclitaxel)则利用人血清白蛋白的自然转运特性,通过gp60受体介导的内皮细胞跨膜转运,使疾病组织药物浓度提高3.3倍,单药剂量可从传统制剂的175mg/m²提升至260mg/m²,且无需预处理。临床研究显示,在转移性乳腺疾病医治中,nab-Paclitaxel组客观缓解率达48%,明显高于传统制剂的26%。此外,针对耐药问题开发的紫杉醇聚合物胶束,通过PEG-PLGA嵌段共聚物形成纳米颗粒,将药物包裹于疏水重要,实现了EPR效应(增强渗透与滞留效应)下的靶向递送,使疾病组织药物蓄积量提高5.8倍。长春艾沙佐咪
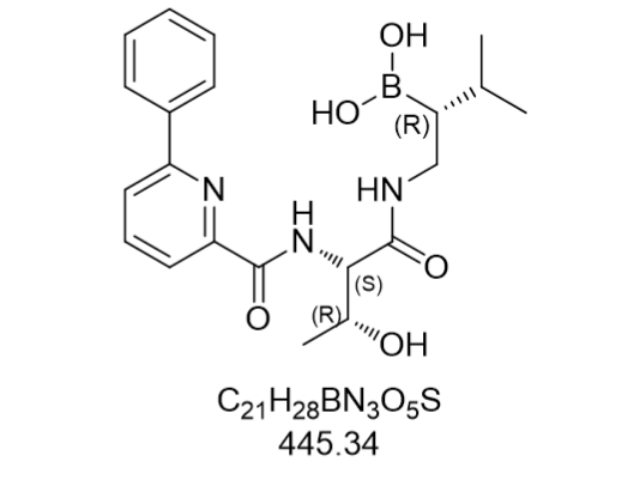
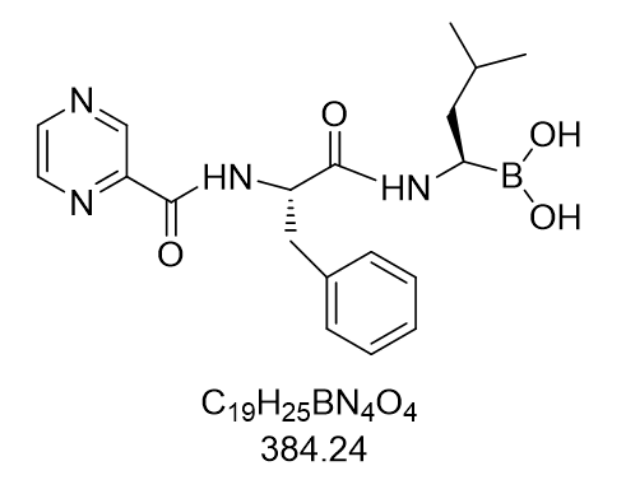
从药代动力学特征分析,德兰佐米的口服生物利用度达62%,明显优于硼替佐米的35%,这得益于其优化的分子极性(LogP=2.1)和肠道吸收特性。在C57BL/6小鼠模型中,单次口服10 mg/kg后,血浆Cmax达1.2 μM,T1/2为6.8小时,较静脉注射硼替佐米的3.2小时延长一倍。组织分布研究显示,德兰佐米在疾病组织的AUC0-24h是正常肌肉组织的3.7倍,这种靶向富集效应与其通过EPR(增强渗透与滞留)效应穿透疾病血管内皮密切相关。代谢稳定性方面,该化合物在肝微粒体中的半衰期为45分钟,主要代谢产物M1(去甲基化衍生物)保留85%的母体活性,形成有效的代谢启动循环。值得注意的是,德兰...


- 长春艾沙佐咪 03-13
- 上海化妆品添加剂供应价格 03-13
- 苏州甲萘醌-4现货 03-13
- 重庆德兰佐米 03-12
- APS-5化学发光底物售价 03-12
- 郑州4-甲基伞形酮酰磷酸酯 03-12
- 艾沙佐咪生产厂家 03-12
- 原料药现价 03-12
- 卡巴他赛供应商 03-12
- 呼和浩特二碘-N-乙酰基酪氨酸乙酯 03-11