随着分子生物学的发展,**免疫组织化学(IHC)染色** 在病理切片分析中占据了**地位。IHC 利用特异性的抗原-抗体结合原理,将目标分子在组织中的定位可视化。常用的方法是使用与目标蛋白结合的一抗,再通过带有酶(如 HRP)的二抗显色。DAB 显色产物在显微镜下呈棕黄色,常与苏木精复染以增强对比度。IHC 可检测**标志物(如 p53、Ki-67、HER2)、炎症因子(如 TNF-α、IL-6)、细胞分化标志物等,既有助于临床诊断,也能为科研提供定量或半定量分析。Trichrome染色用于区分胶原、肌肉和细胞核。阿里辛蓝染色效果

病理切片染色的效果在很大程度上依赖于前期的制备过程。通常包括组织取材、固定、脱水、包埋、切片和脱蜡等步骤。组织固定最常见的是 4% 多聚甲醛或 10% 中性甲醛溶液,能够保持组织结构稳定,防止自溶。石蜡包埋后使用切片机将组织切至 3–5 μm 厚度,再铺展于载玻片上。正式染色前,还需要进行脱蜡和水化,以去除石蜡并恢复组织的亲水性,为后续染色做好准备。如果这些步骤不规范,往往会导致染色不均匀或背景过重,从而影响观察结果。免疫组化染色公司镀银染色用于显示神经纤维和基底膜。

除了基础染色,病理实验中常常需要进行一些特殊染色,以满足研究和诊断的需求。比如 **普鲁士蓝染色** 用于检测铁沉积,可帮助诊断血色病或出血后铁积聚;**刚果红染色** 可用于识别淀粉样蛋白沉积,在偏光显微镜下呈现典型的苹果绿双折光;**油红O 染色** 则用于脂质检测,常见于***或脂肪变性研究。这些特殊染色方法能够揭示组织中的特定成分,对于疾病的分型和机制探索有着重要意义。专业染色切片平台,各类染色检测,提供原始图片,原始数据。
普鲁士蓝染色的注意事项•对照设置:为了确保结果的准确性,应设置阳性对照(已知含铁的样本)和阴性对照(不含铁的样本)。•背景信号:有时会出现非特异性的背景信号,需要注意优化实验条件以减少背景噪声。•固定和通透性:正确的固定和通透处理对于获得良好的染色结果至关重要。总结鲁士蓝染色是一种经典的组织化学染色方法,广泛应用于检测和定位组织中的铁沉积。它在铁代谢相关疾病、神经退行性疾病和**研究等领域具有重要应用价值。通过鲁士蓝染色,研究人员可以获得关于铁沉积的详细信息,从而更好地理解疾病的发病机制和病理变化。Giemsa染色广泛应用于血液涂片和骨髓涂片。
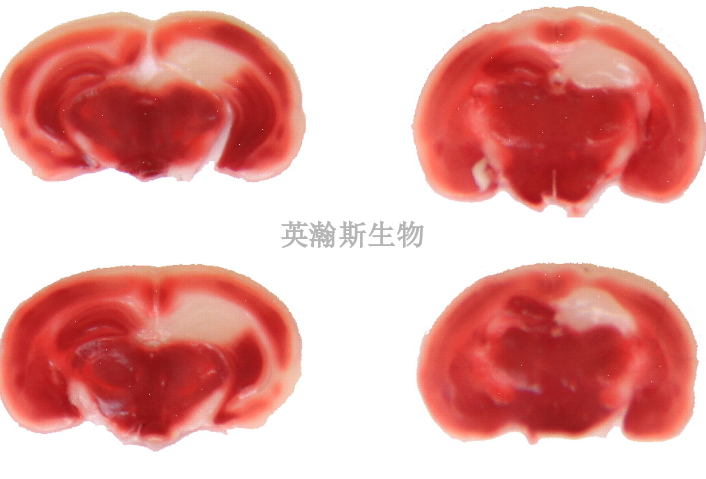
在组织病理切片染色中,染色效果的优劣直接关系到后续实验数据的可靠性。良好的染色应呈现对比鲜明、结构清晰的图像,细胞核、胞质和组织基质应层次分明。病理切片染色过程中需注意试剂浓度、温度和时间的严格控制,不同组织或目标分子对染色条件的要求可能不同。例如,小鼠脑组织切片在免疫荧光染色中往往需要延长抗原修复时间,以便提高抗体结合效率。切片染色不仅是技术活,更是对实验设计和动手能力的综合考验。专业病理实验平台苏木精-伊红(H&E)染色是常用的组织学染色方法。免疫组化染色公司
染色切片帮助展示动物模型的病理变化。阿里辛蓝染色效果
切片染色的实验检测流程通常包括脱蜡、水化、染色、脱水、透明和封片等多个步骤。每一步都需精确控制时间与操作细节,尤其是在石蜡切片的处理过程中,脱蜡不彻底可能导致染色不均或背景过强。水化后染色阶段要根据染色类型选择合适的染料和缓冲液。病理切片染色完成后进行脱水和透明处理,一般使用梯度酒精和二甲苯,再用中性树胶封片。整个流程需在无尘、无振动的环境下操作,才能获得高质量的成像结果。切片染色实验需要有经验的成熟病理团队来完成。阿里辛蓝染色效果