在对药物临床有效性研究资料的审评中应关注的问题:1.研究设计的整体考虑(假设、缺乏对照数据、实验室检测的不足);2.关键数据的分析、所提供研究的选择;3.终点的选择(包括等级量表)、终点测量的合法性;4.对照药的选择;5.人群的选择(儿童或不符合要求的患者);6.入选的患者过少;7.疗程不够长;8.缺乏长期随访的数据;9.临床研究数据的合法性(主要方案的违背或其他GCP问题);10.与临床疗效相关的剂量方案确定;11.缺乏与临床疗效相关的特异的相互作用的研究(包括合并用药和中和抗体);12.观察到的与适应症相关的临床有效性大小的关系问题:边缘/无临床相关疗效(包括疗效的持续时间、)与临床疗效不一致、对临床有效性的其他关注问题(药效学腐代动力学与现有比较的学定位)。斑马鱼实验模型-药物、化妆品功效评价。药物安全性评价多少钱
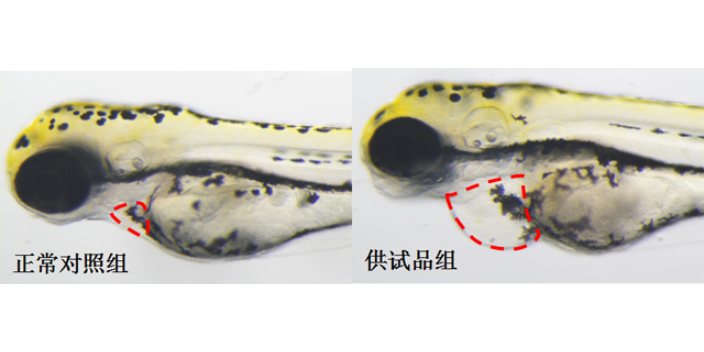
利用斑马鱼模型评价保护肾脏功效。肾脏是人体的重要组成部分,,发挥着从血液中滤过代谢废物并维持体内正常酸碱和渗透压平衡的重要作用。斑马鱼的肾脏与哺乳动物肾脏的发育及疾病的发生、发展存在很多相似之处,涉及的许多基因具有高度保守性。因此,斑马鱼适合用于评价保护肾脏功效。马兜铃酸主要损伤肾小管上皮细胞,导致肾间质纤维化及肾萎缩,并出现低分子蛋白尿、严重贫血症状,被称为“马兜铃酸肾病”。在人体和斑马鱼上,马兜铃酸均可诱发肾性水肿和肾脏形态功能异常,引起不可逆性肾损伤并至死亡。评价保护肾脏功效有两个指标:1.肾性水肿发生率。由于斑马鱼通体透明,肾性水肿可以明显的被观察到。2.肾小球滤过率。通过注射荧光物质,正常斑马鱼可将荧光物质排出体外,肾小球滤过功能损伤的斑马鱼不能将荧光物质排出体外。观察斑马鱼全身荧光强度可分析肾小球滤过率。药理药效实验斑马鱼模型评价肾脏毒性。
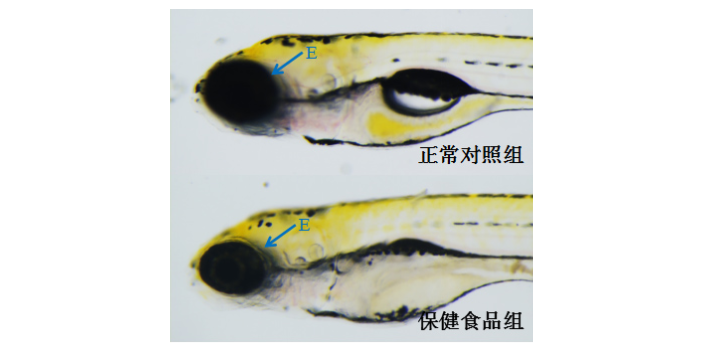
斑马鱼胃肠道粘膜屏障系统由较完整的机械屏障、化学屏障和免疫屏障构成,与哺乳动物高度相似,可作为胃肠道粘膜屏障研究的动物模型。三******磺酸(TNBS)可破坏肠道粘膜屏障,与肠组织蛋白结合形成抗原,发生变化反应,诱发结肠炎。杯状细胞主要分泌黏蛋白,形成黏膜屏障以保护上皮细胞,肠黏膜损伤时杯状细胞数量减少。我们可以应用特异性的染料(呈蓝色),观察肠道杯状细胞数目,评价肠道粘液分泌功能。 我们将受测试斑马鱼分成三组,分别是正常对照组、模型对照组和服用肠道粘膜辅助保护剂组。其中正常对照组未经任何处理,模型对照组与服用肠道粘膜辅助保护剂组都摄入了等量的TNBS(TNBS通过溶解到养鱼用水中的方式摄入到斑马鱼体内)。服用肠道粘膜辅助保护剂组在TNBS诱导肠道粘膜损伤之后摄入类似的肠道粘膜辅助保护剂。服用一段时间肠道粘膜辅助保护剂后,我们观察和分析肠道杯状细胞数目。
由于硬骨鱼和人类在骨骼发育过程中的基因、信号通路有高度同源性,而且与其他的动物模型相比,斑马鱼具有个体小适合高通量化学筛选、幼鱼身体透明易于观察骨骼发育的特点,所以近年来以斑马鱼为模型的骨骼研究逐渐成为这一领域的热点。斑马鱼从前向后的脊椎发育过程是非连续的,而是分成两个不同的区域:前域(包括第3块椎骨)和后域(包括第4-31块椎骨)。将斑马鱼脊椎骨钙化过程分成两个不同区域是基于第2和第3椎骨的出现晚于第4椎骨。我们利用斑马鱼骨骼发育的规律,摄入生长发育促进剂的斑马鱼脊椎骨发育会加快。脊椎骨染色应用与钙特异性结合的荧光染料(呈绿色),经荧光显微镜观察脊椎骨的数量。利用斑马鱼模型评价心血管毒性。
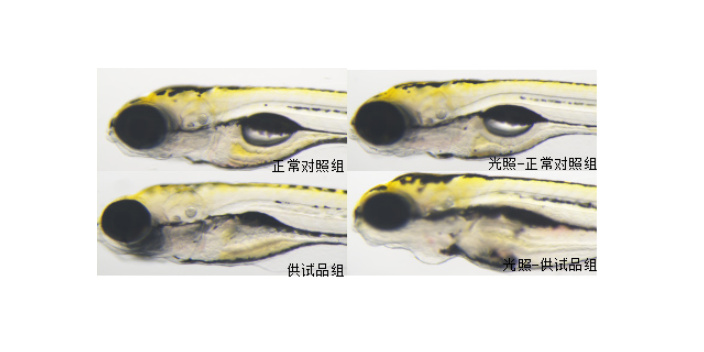
静脉注射给予长春瑞滨造模斑马鱼抵抗力低下模型。大剂量长春瑞滨骨髓抑制明显,导致血小板、红细胞及白细胞数目(中性粒细胞、巨噬细胞、T细胞等)减少和贫血,导致抵抗力低下。人类与斑马鱼在免疫系统的细胞组成上极为相似,而且斑马鱼是目前所有同时具有特异性免疫和非特异性免疫动物个体中体积较小的,适合高通量评价调节免疫功效。斑马鱼静脉注射大剂量长春瑞滨后可造成免疫低下。采用转基因T细胞红色荧光斑马鱼,可在荧光显微镜在观察到抵抗力低下的斑马鱼体内的T细胞荧光强度明显减弱斑马鱼模型评价促进组织再生伤口愈合功效。药理药效实验
利用斑马鱼模型评价抗焦虑功效。药物安全性评价多少钱
我们将受测试斑马鱼分成三组,分别是底物对照组、正常对照和服用供试品组(供试品通过溶解到养鱼用水中摄入到斑马鱼体内),并加入ROS特异性荧光检测试剂。服用供试品一段时间后,我们使用酶标仪对斑马鱼体内ROS进行荧光定量。可以看到,服用供试品组斑马鱼体内荧光值比正常对照组有明显升高。1.经过每组30尾斑马鱼的对比实验,服用供试品组的斑马鱼ROS水平明显高于正常对照组,与正常对照组存在明显性差异。2.本实验证实了该供试品诱发斑马鱼氧化应激。药物安全性评价多少钱