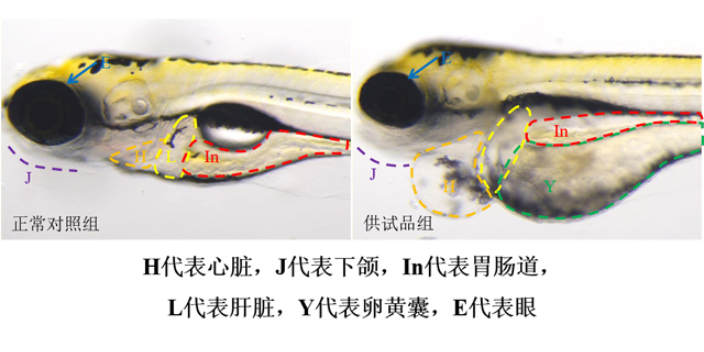
尽管技术进步明显,药物筛选仍面临多重挑战。一是靶点验证困难,约70%的临床试验失败源于靶点选择错误,需结合基因编辑、单细胞测序等技术深化机制研究;二是多靶点药物筛选复杂,慢性病(如糖尿病、阿尔茨海默病)需同时调控多个通路,传统方法难以兼顾;三是数据整合挑战,生物医学数据分散于不同数据库,格式、标准不统一,需构建统一的数据中台。未来,药物筛选将向“系统药理学”方向发展,结合多组学(基因组、转录组、代谢组)、网络药理学和真实世界数据(RWD),构建“靶点-通路-疾病”的动态模型。例如,通过患者电子病历、可穿戴设备数据,实时监测药物疗效与安全性,实现“精细筛选-个性化用药”的闭环。随着技术的融合与创新,药物筛选正从“发现药物”迈向“发现疗愈方案”。利用斑马鱼模型评价改善心脏出血功效。中药功效与安全性评价
中药抗tumor研究已从直接杀伤细胞转向表观遗传调控领域。以黄芩苷为例,其可通过抑制组蛋白去乙酰化酶(HDAC)活性,上调p21基因表达,诱导肿瘤细胞周期阻滞。实验显示,黄芩苷处理后的肝ancer细胞,其H3K27ac修饰水平明显升高,促进抑ancer基因转录。另一机制是中药多糖对DNA甲基化的调节,如茯苓多糖可降低结直肠癌细胞中DNMT3B表达,恢复MLH1等抑ancer基因的甲基化沉默。此外,中药复方(如四君子汤)可通过调节miRNA表达(如上调miR-34a),抑制tumor干细胞自我更新。这些表观遗传调控研究,为中药抗tumor提供了新的分子靶点,也解释了其“多靶点、低毒性”的优势。药物研发科研服务利用斑马鱼模型评价抗焦虑功效。
在科技日新月异的现在,人类对罕见病的研究与医疗不断取得新的突破。肌萎缩侧索硬化症(Amyotrophiclateralsclerosis,ALS),作为一种目前仍无法痊愈的、具有临床异质表现的多基因、多因素、进行性的神经退行性疾病,其特征是上、下行运动神经元丢失。斑马鱼,由于其与人类基因高度相似、胚胎透明、遗传操作便利等特点,不仅可实现不同细胞的可视化从而观察运动神经元或肌肉细胞的病变,而且可高通量检测和分析运动相关的行为学改变,为探索ALS中运动障碍的病理机制、筛选新的潜在药物、发现临床新疗法等提供了良好的工具,呈现出巨大的应用潜力。
中药药效评价需结合体内外实验模型,验证其医疗作用。体外实验常用细胞模型,如人肝ancer细胞HepG2用于评估中药抗tumor活性。例如,研究发现黄连素可通过诱导细胞凋亡抑制肝ancer细胞增殖。体内实验则依赖动物模型,如糖尿病小鼠模型用于测试中药降糖效果。例如,六味地黄丸可明显降低糖尿病小鼠的空腹血糖和糖化血红蛋白水平。此外,网络药理学技术通过整合多组学数据,预测中药与靶点的相互作用,为实验设计提供方向。例如,通过构建“成分-靶点-疾病”网络,发现黄芪多糖可能通过调节PI3K/Akt信号通路发挥免疫调节作用。斑马鱼模型实验评价细胞凋亡。
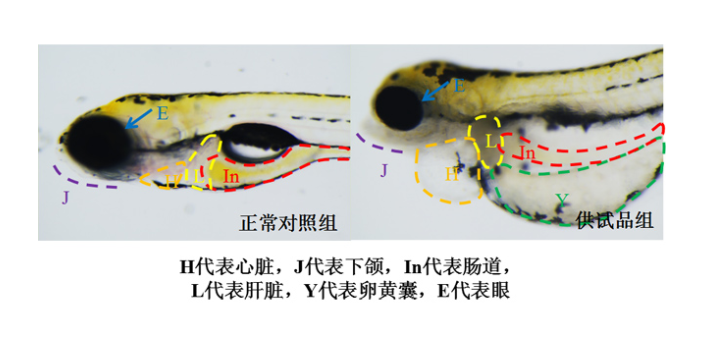
线粒体功能障碍是神经退行性疾病的关键病理,而中药可通过调节线粒体动态(融合/分裂)发挥保护作用。以石杉碱甲为例,其可抑制Drp1蛋白活性,减少线粒体过度分裂,维持神经元线粒体网络稳定性。实验显示,石杉碱甲处理后的阿尔茨海默病模型小鼠,其海马区线粒体嵴结构完整率提高40%,认知功能明显改善。另一机制是中药对线粒体自噬的调节,如黄芪多糖可启动PINK1/Parkin通路,清理受损线粒体,减少神经元凋亡。此外,中药复方(如六味地黄丸)可通过调节线粒体生物发生相关基因(如PGC-1α),促进线粒体再生。这些研究为中药医疗神经退行性疾病提供了线粒体水平的机制解释。利用斑马鱼模型评价改善贫血功效。生物安全性评价
斑马鱼模型评价促进组织再生伤口愈合功效。中药功效与安全性评价
中药活性成分的精细分离是现代中药研究的基础。传统方法如溶剂萃取、柱层析存在效率低、选择性差等问题,而超临界流体萃取(SFE)与高速逆流色谱(HSCCC)的联用技术,明显提升了分离效率。例如,从丹参中分离丹参酮IIA时,SFE以CO₂为溶剂,在35℃、25MPa条件下实现98%的提取率,较传统方法提升3倍。HSCCC则通过液液分配系数差异,将丹参酮IIA纯度提升至99.2%。结构鉴定方面,冷喷离子化质谱(CSI-MS)与核磁共振(NMR)的联用,可快速确定复杂成分的立体构型。如从三七中分离的新皂苷Rg₅,通过2DNMR谱图解析其糖链连接方式,为活性评价提供了结构依据。这些技术突破,使中药活性成分研究进入“微量、精细、高效”的新阶段。中药功效与安全性评价