中药对免疫系统的调节作用常涉及细胞因子网络的动态平衡。以雷公藤甲素为例,其可通过抑制NF-κB通路,下调TNF-α、IL-6等促炎因子,同时上调IL-10、TGF-β等抑炎因子,缓解类风湿关节炎症状。实验显示,雷公藤甲素处理后的佐剂性关节炎大鼠,其关节肿胀度较对照组降低60%。另一机制是中药对T细胞亚群的调节,如黄芪多糖可促进调节性T细胞(Treg)分化,抑制Th17细胞过度活化,维持免疫耐受。此外,中药复方(如玉屏风散)可通过调节肠道菌群,影响短链脂肪酸(如丁酸)产生,间接调节免疫细胞功能。这些细胞因子网络研究,为中药免疫调节提供了系统生物学视角。新一轮基本药物目录调整在即。药物药学实验
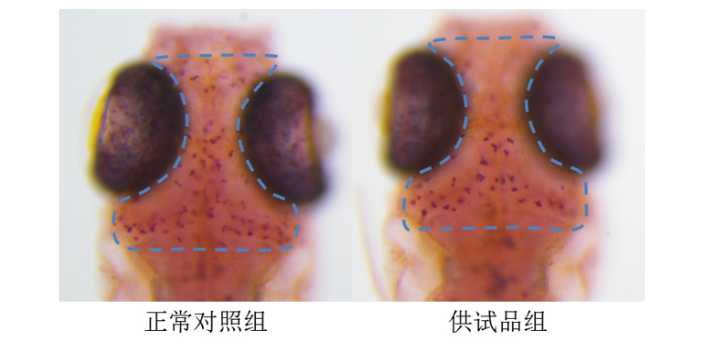
中药药效评价需结合体内外实验模型,验证其医疗作用。体外实验常用细胞模型,如人肝ancer细胞HepG2用于评估中药抗tumor活性。例如,研究发现黄连素可通过诱导细胞凋亡抑制肝ancer细胞增殖。体内实验则依赖动物模型,如糖尿病小鼠模型用于测试中药降糖效果。例如,六味地黄丸可明显降低糖尿病小鼠的空腹血糖和糖化血红蛋白水平。此外,网络药理学技术通过整合多组学数据,预测中药与靶点的相互作用,为实验设计提供方向。例如,通过构建“成分-靶点-疾病”网络,发现黄芪多糖可能通过调节PI3K/Akt信号通路发挥免疫调节作用。体外药效学研究斑马鱼模型实验评价细胞凋亡。
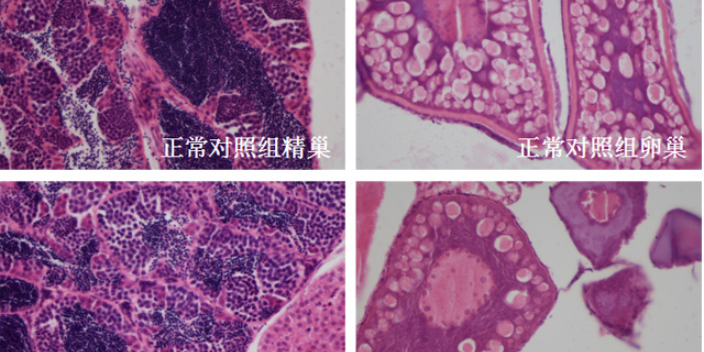
中药复方通过多成分、多靶点、多途径发挥疗效,但其作用机制长期存在“黑箱”问题。网络药理学技术的引入,为解析复方机制提供了新范式。以经典方剂“补阳还五汤”为例,研究者通过数据库挖掘其127种化学成分,结合靶点预测算法,筛选出与神经保护相关的关键靶点(如VEGF、BDNF)。进一步通过分子对接验证,发现黄芪甲苷、川芎嗪等成分可稳定结合PI3K/Akt通路关键蛋白,启动神经元存活信号。实验验证显示,该复方能显著提高脑缺血大鼠海马区神经元密度,且作用强度与单体成分联用相当,揭示了复方“协同增效”的科学内涵。这种“成分-靶点-通路-表型”的系统研究模式,正推动中药从经验医学向精细医学转型。
药物研究中的药代动力学(ADME)研究是评估药物体内吸收、分布、代谢、排泄特性的关键内容,是药物研究中决定药物临床应用前景的关键环节。杭州环特生物建立了基于斑马鱼的药物研究药代动力学评价体系,为小分子药物研究提供快速、高效的ADME研究服务。斑马鱼体型小、胚胎透明、药物暴露方式简单(水体浸泡或显微注射),在药物研究中可实现对药物体内过程的实时、动态监测。通过高分辨质谱、荧光标记、分子影像学等技术,环特生物在药物研究中精细测定药物在斑马鱼体内的浓度变化、组织分布、代谢产物及排泄途径,获取关键药代动力学参数。斑马鱼药物研究ADME模型与人类具有高度相关性,可在药物研究早期快速评估化合物的药代特性,为药物研究中的候选药物筛选与优化提供重要依据。斑马鱼模型评价胃肠道毒性。
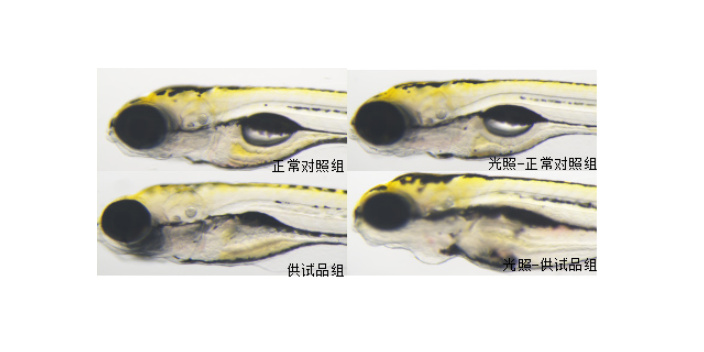
药物研究中的耐药性研究是tumor、影响性疾病等领域药物研究的重大挑战,克服耐药性是提升药物研究临床价值的关键。杭州环特生物依托斑马鱼药物研究模型,建立了完善的药物耐药性药物研究体系,为克服耐药性的小分子药物研究提供高效工具。在药物研究中,通过长期药物诱导构建tumor、病原菌等斑马鱼耐药药物研究模型,模拟临床耐药发生过程;利用斑马鱼模型开展耐药机制研究,解析药物靶点突变、信号通路jihuo、药物外排等耐药分子机制;同时筛选与评价可逆转耐药的新型小分子化合物或联合用药的方案。斑马鱼耐药药物研究模型具有造模快、成本低、可可视化观察等优势,为耐药性药物研究提供了强大的体内研究平台,助力开发克服耐药的创新小分子药物。利用斑马鱼模型评价糖尿病神经炎症消退功效。新药安全性评价方案
利用斑马鱼模型实验评价通便功效。药物药学实验
随着分子生物学技术的不断发展,其在药品机理研究中发挥着越来越重要的作用。基因编辑技术如CRISPR-Cas9的出现,使科研人员能够精细地对细胞或动物模型的基因进行敲除、插入或修改,从而研究特定基因与药物作用之间的关系。例如,通过敲除细胞中的某个基因,观察药物对细胞功能的影响是否改变,以此确定该基因是否为药物作用的靶点或相关调控基因。蛋白质组学技术则可多方面分析药物作用后细胞内蛋白质的变化情况,通过质谱技术鉴定蛋白质的种类、修饰状态及表达量变化,帮助发现药物作用的新靶点和潜在机制。此外,荧光标记技术能够实时追踪药物在细胞内的运输路径、与靶点的结合过程,直观地展现药物发挥作用的动态过程。这些分子生物学技术从基因和蛋白质水平深入解析药物作用机理,极大地推动了药品机理研究的发展,为创新药物研发提供了有力的技术支撑。药物药学实验