展望未来,小分子药物研究将在技术创新、需求驱动与全球合作的推动下迎来更广阔的发展空间,杭州环特生物将持续带动斑马鱼药物研究技术创新,深耕小分子药物研究领域,为全球药物研究事业贡献关键力量。环特生物将进一步升级 “六位一体”药物研究平台,深化 AI、类organ、基因编辑等前沿技术与斑马鱼药物研究的融合,拓展药物研究疾病领域与技术服务范围;持续优化药物研究质量体系、提升药物研究效率、降低药物研究成本,为全球客户提供更高效、更精细、更可靠的小分子药物研究解决方案;积极推动药物研究全球合作、成果转化与行业标准化建设,助力攻克更多疑难病症、提升人类健康水平,成为全球小分子药物研究值得信赖的合作伙伴与技术带动者。利用斑马鱼模型评价心血管毒性。中药药效实验费用
药物研究的突破离不开创新技术与多学科交叉融合,人工智能与模式生物的结合正重塑小分子药物研究的未来格局。杭州环特生物积极布局AI驱动的药物研究技术,将深度学习、分子模拟与斑马鱼药物研究平台深度融合,构建智能化药物研究新体系。在药物研究的靶点发现阶段,AI算法通过挖掘海量生物医学数据,精细预测疾病相关靶点与潜在药物分子;在药物研究的分子设计阶段,生成式AI快速构建全新小分子库,再通过斑马鱼药物研究模型进行体内活性验证,形成“AI预测—斑马鱼验证—结构优化”的闭环药物研究流程。环特生物的AI+斑马鱼药物研究平台,将传统药物研究中数年的筛选周期压缩至数周,明显提升药物研究效率,带动药物研究进入智能化、精细化新时代。药品安评中心利用斑马鱼模型评价镇痛作用。
药物研究中的耐药性研究是tumor、影响性疾病等领域药物研究的重大挑战,克服耐药性是提升药物研究临床价值的关键。杭州环特生物依托斑马鱼药物研究模型,建立了完善的药物耐药性药物研究体系,为克服耐药性的小分子药物研究提供高效工具。在药物研究中,通过长期药物诱导构建tumor、病原菌等斑马鱼耐药药物研究模型,模拟临床耐药发生过程;利用斑马鱼模型开展耐药机制研究,解析药物靶点突变、信号通路jihuo、药物外排等耐药分子机制;同时筛选与评价可逆转耐药的新型小分子化合物或联合用药的方案。斑马鱼耐药药物研究模型具有造模快、成本低、可可视化观察等优势,为耐药性药物研究提供了强大的体内研究平台,助力开发克服耐药的创新小分子药物。
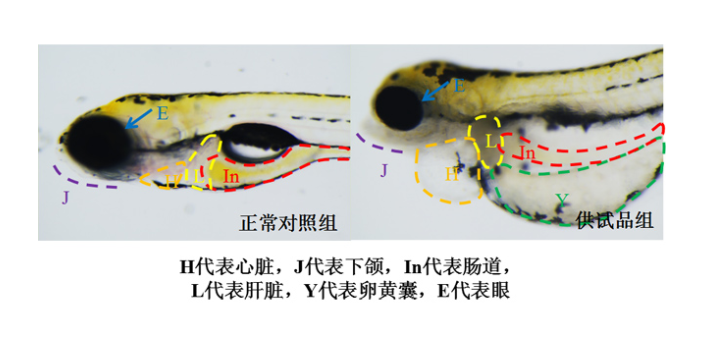
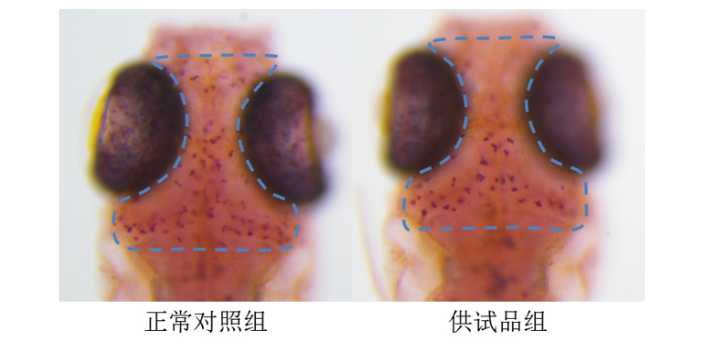
表观遗传调控,如DNA甲基化,通过干扰脂质代谢在人类肥胖发展中发挥作用。我们假设TBPH破坏代谢处理器,通过PPAR信号导致脂质稳态受损通路;然而,TBPH对脂质代谢的生物学作用仍有待阐明。据报道,许多环境污染物会破坏动物体内的脂质稳态,导致异常的脂质积累,主要是肝细胞中甘油三酯(TG)的积累,并伴随肝细胞膨胀、炎症和氧化应激。这些不良反应可能导致肝脂肪变性或从单纯性脂肪肝转变为代谢综合征的肝脏表现,如非酒精性脂肪性肝病(NAFLD)的组织学表型。利用斑马鱼模型评价抗焦虑功效。

神经退行性疾病药物研究面临靶点难发现、血脑屏障穿透难、临床转化效率低等重大挑战,是药物研究领域的难点与焦点。杭州环特生物凭借斑马鱼在神经药物研究中的独特优势,构建了帕金森病、阿尔茨海默病、癫痫等多种神经疾病斑马鱼药物研究模型,为神经小分子药物研究开辟新路径。斑马鱼的中枢的神经系统发育与人类高度保守,具有血脑屏障结构,且行为学表型易观测,在药物研究中可实现对神经保护、神经修复、神经递质调节等药物效果的精细评估。在药物研究中,环特生物通过分子标记、行为学分析、电生理检测等技术,多方面解析药物研究中化合物的神经药理活性与作用机制,突破传统神经药物研究体外模型与哺乳动物模型的局限,为攻克神经退行性疾病提供高效药物研究平台。斑马鱼模型评价促进组织再生伤口愈合功效。原研药物的安全性评价
药物功效评价-药物毒性安全性评价项目 。中药药效实验费用
研究人员在116名患者的376种类organ中筛选出7种PLC相关药物,包括前列药物乐伐替尼(lenvatinib)和索拉非尼(sorafenib),二线药物瑞格拉非尼(reorafenib)和阿帕替尼(apatinib),anti-VEGFR抗体贝伐单抗(bevacizumab),以及靶向具有可操作突变的ICC药物,包括佩米替尼(pemigatinib,靶向含FGFR2融合/重排的胆管cancer)和艾伏尼布 (ivosidenib,靶向IDH1突变的化疗难治性胆管cancer)。结果显示,7种筛选药物的IC50和AUC值之间存在很强的相关性。接着,研究人员基于类organ药物敏感性结果与相应临床反应进行比较,发现临床反应支持使用类organ的乐伐替尼(lenvatinib)敏感性结果,与索拉非尼(sorafenib)、阿帕替尼(apatinib)的类似比较,也证实了类organ药物筛选的预测价值。中药药效实验费用