我们将受测试斑马鱼分成三组,分别是正常对照组、模型对照组和抗心衰药物组。其中正常对照组未摄入维拉帕米,模型对照组与抗心衰药物组都摄入了等量的维拉帕米(维拉帕米通过溶解到养鱼用水中的方式摄入到斑马鱼体内)。抗心衰药物组在摄入维拉帕米的同时加入地高辛、美托洛尔类的抗心衰药物。服用一段时间抗心衰药物后,观察斑马鱼心包水肿和静脉淤血的情况;用心跳血流分析系统检测心搏出量和血流速度的情况。可以看到,服用抗心衰药物组的心包面积和静脉瘀血面积与未摄入维拉帕米的正常对照组基本相似,没有明显的心衰情况。斑马鱼模型评价半数致死浓度。北京药物安全性评价单位
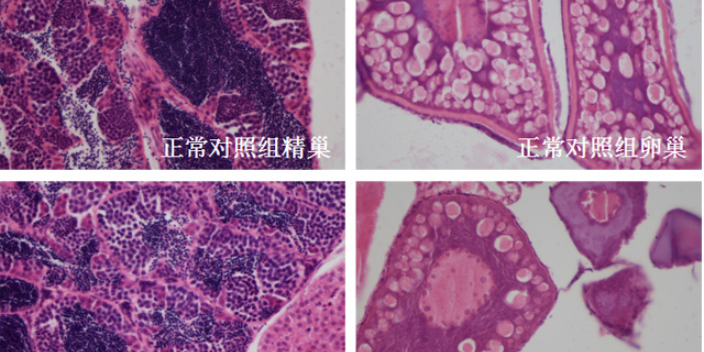
我们将受测试斑马鱼分成三组,分别是正常对照组、模型对照组和服用肝保护剂组。其中正常对照组未摄入乙醇,模型对照组与服用肝保护剂组都摄入了等量的乙醇(乙醇通过溶解到养鱼用水中的方式摄入到斑马鱼体内)。肝保护剂组在摄入对乙醇的同时摄入美他多辛之类的肝保护剂。服用一段时间肝保护剂后,我们在显微镜下观察斑马鱼肝脏及卵黄囊表型,同时制作成病理切片观察肝脏的病理结构变化。从病理切片中也能看出来,正常对照组肝细胞核规则清晰,肝细胞结构正常,边缘清晰。乙醇处理后,斑马鱼肝细胞结构模糊、肝细胞核肿大,肝组织出现脂肪空泡样变性,而肝保护剂组细胞和正常斑马鱼中形态相似。普通药物评价利用斑马鱼模型评价改善贫血功效。
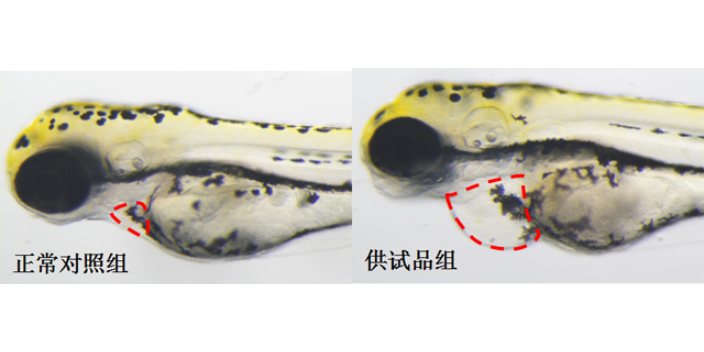
脑出血是指非外伤性脑实质内部血管破裂引发的脑内出血病症,占全部脑卒中的20%~30%,急性期病死率为30%~40%。羟甲基戊二酸单酰辅酶A还原酶(HMGCR)是他汀类药物发挥抑制作用的直接作用点,HMGCR功能被抑制会影响血管的完整性和稳定性,诱发脑出血。由于斑马鱼大脑具有典型脊椎动物脑部形态学特征,血管与神经系统在分子信号通路上与人和哺乳动物的同源性达到85%以上。在大量摄入辛伐他汀后,斑马鱼脑部也会出现脑出血的情况,患有脑出血的斑马鱼的脑部会出现明显的片状出血,而正常斑马鱼没有;由于脑出血斑马鱼的心搏输出量和血流速度也会降低,利用血流分析仪可明显观察到。脑出血可直接造成反应迟钝、运动功能障碍,可通过行为分析软件观察斑马鱼的行为轨迹。我们评价斑马鱼脑出血有4个指标:1.脑出血发生率;2.心搏输出量;3.血流速度;4.行为学(运动改善)。
药物评价是研究药物与人体之间的相互作川及其规律。药物安全性评价的重要性任何药物都具有两重性,如药物,它一方面可以杀灭病源菌,使病人的生理,生化机能恢复正常,另一方面也可危害机体,产生不良反应.尤其是20世纪60年代初,在欧洲发生反应停(thalidomide)事件,累及28个国家后,对药物的安全性评价,引起各国和世界卫生组织的高度重视.近年来,在新药临床试验中,要实施新药临床试验规范(Good Clinical Practice,GCP),执行赫尔辛基宣言,保护受试者权益,使病人在药物治疗中获得比较大效益,而冒小风险.因此对药物进行评价,药物的有效性和安全性两者应放在同等位置,均不容忽视.斑马鱼模型评价眼毒性。
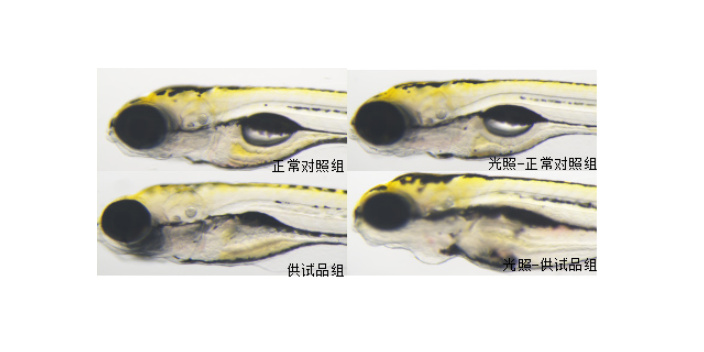
与药效学相关的临床前药代动力学研究,其目的在于揭示新药在动物体内的动态变化规律,阐明药物的吸收、分布、代谢和排泄的过程和特点。临床前药代动力学研究也是支持立题依据的重要内容,药物在体内的吸收、分布、代谢和排泄情况与药物的实际疗效及安全性密切相关,因此进行临床前药代动力学研究时不能孤立于药效学和毒理研究之外,从试验设计到结果评价都要与之紧密结合,充分发挥桥接作用。其意义在于:1.解释动物毒性研究结果,帮助完善毒理研究的设计。2.解释药效学研究结果,提示药物相互作用可能性的信息。3.提供药效和毒性反应种属差异的药代动力学原因。4.为给药途径和剂型等改变提供安全性、有效性与剂量相关性的依据。5.为临床研究(I期药代)提供参考。利用斑马鱼模型评价帕金森病防治作用。药效评价研究方案
斑马鱼模型评价听毒性。北京药物安全性评价单位
肠道消化是食物在消化道中分解的过程,包括机械性消化(通过消化道肌肉搜索将食物与消化液混合并向消化道远端推送)和化学性消化(通过消化腺分泌的消化酶将大分子分解为小分子物质的过程)。肠道内的消化液包括胰脂肪酶、胰蛋白酶、胰淀粉酶等。在受精后的26-126h,斑马鱼肠道的管腔形成,内胚层分化出连续的有功能的肠道上皮。斑马鱼肠道肌肉发达,可分为两层平滑肌,有利于食物的蠕动消化。通过特异性的检测试剂盒检测OD值,可以量化斑马鱼体内胰脂肪酶和胰蛋白酶含量。北京药物安全性评价单位